Hepatit B Virus DNA
Düzeyi Tayini ve Eş Zamanlı Olarak
YMDD Motif Mutasyonu Analizi Yapan Gerçek Zamanlı PCR Testi*
A
Real-Time PCR Assay for the Quantification of Hepatitis B Virus DNA and
Concurrent Detection of YMDD
Motif Mutations
Harun AĞCA1, A. Arzu SAYINER2, Aylin ŞENGÖNÜL2, İlkay ŞİMŞEK3, Mesut AKARSU3
1 Kütahya Doç. Dr. Mustafa Kalemli Tavşanlı Devlet Hastanesi, Mikrobiyoloji Laboratuvarı, Kütahya.
1 Kutahya Doç. Dr. Mustafa Kalemli Tavsanli State Hospital, Microbiology Laboratory, Kutahya, Turkey.
2 Dokuz Eylül Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, İzmir.
2 Dokuz Eylul University Faculty of Medicine, Department of Medical Microbiology, Izmir, Turkey.
3 Dokuz Eylül Üniversitesi Tıp Fakültesi, Gastroenteroloji Bilim Dalı, İzmir.
3 Dokuz Eylul University Faculty of Medicine, Department of Gastroenterology, Izmir, Turkey.
* Bu çalışma Dokuz Eylül Üniversitesi Bilimsel Araştırma Fonu tarafından desteklenmiştir.
ÖZET
Kronik hepatit B enfeksiyonu tedavisi için lamivudin alan hastalarda tedavi takibinde genotipik yöntemler ve viral DNA düzeyi tayini yöntemleri kullanılmakta olup, yoğun bir iş yükü ve uzun bir zaman gerektirmektedir. Bu çalışmada, aynı testte eş zamanlı olarak hepatit B virusu (HBV) DNA düzeyi tayini ve YMDD (tirozin, metionin, aspartat, aspartat) motif mutasyonu analizini gerçekleştirebilecek yeni bir test geliştirilmesi hedeflenmiştir. Test, YMDD motifine özgü hibridizasyon probu temelli gerçek zamanlı polimeraz zincir reaksiyonu (Rt-PCR) ile gerçekleştirilmiştir. YMDD motifinin belirlenmesi için erime noktası sıcaklığı analizi kullanılmıştır. HBV-DNA düzeyi 1000 ile 3 milyon kopya/ml arasında değişen standart serum örneklerinin (VQC S2220) çalışılmasıyla elde edilen standart eğri kullanılarak viral DNA düzeyi tayin edilmiştir. Geliştirilen yöntem, viral yük tayininde kullanılan kantitatif ticari bir kit (Artus HBV RG PCR; Qiagen, Almanya), ticari “line prob” (INNO-LiPA HBV DR v1.0; Innogenetics, Belçika) kiti ve DNA dizi analizi yöntemleriyle karşılaştırılmıştır. Çalışmada, kronik hepatit B enfeksiyonu olan ve tek başına lamivudin tedavisi alan, HIV ve HCV antijen ve antikorları negatif 20 hastaya (7 kadın, 13 erkek; yaş aralığı: 27-70 yıl) ait 38 serum örneği test edilmiştir. Geliştirilen yöntemin analitik duyarlılık sınırının 200 kopya/ml, dinamik aralığının ise 1 x 103 ile 3 x 107 kopya/ml arasında olduğu tespit edilmiş; yöntemin PCR etkinliği 1.98 olarak belirlenmiştir. Geliştirilen yöntem ve ticari kit ile elde edilen log10 HBV-DNA kopya/ml değerleri arasında yüksek bir korelasyon saptanmıştır (r= 0.681). Geliştirilen yöntem ile erime noktası sıcaklığı (Tm) analizine göre YMDD motifi mutasyonu araştırılmış ve Tm değeri YMDD için 59.86°C, YVDD için 56.34°C ve YIDD için 55.10°C olarak belirlenmiştir. Homojen viral popülasyon içeren örneklerde, geliştirilen yöntemin sonuçları dizi analizi ve LiPA ile benzer bulunmuş; karışık viral popülasyon içeren serum örneklerinin analizinde ise geliştirilen yöntemin baskın olan viral tipi belirlediği tespit edilmiştir. Sonuç olarak, çalışmamızda geliştirilen bu testin hızlı, güvenilir ve tekrarlanabilir bir biçimde HBV-DNA düzeyi tayini ve YMDD motifi analizini, aynı çalışmada eş zamanlı olarak iki saat süre içinde gerçekleştirebildiği belirlenmiş; bu yöntemin, lamivudin tedavisi almakta olan kronik hepatit B enfeksiyonlu hastaların takibinde kullanılabilecek uygun bir yöntem olduğu düşünülmüştür.
Anahtar sözcükler: Hepatit B virusu; HBV-DNA; lamivudin; direnç; mutasyon; YMDD; gerçek zamanlı polimeraz zincir reaksiyonu.
ABSTRACT
Monitoring therapy in chronic hepatitis B patients receiving lamivudine therapy, is done by two different assays; determination of viral load and genotypic resistance. These methods are labor intensive and time consuming. It was aimed to develop an assay to quantitate hepatitis B virus (HBV) DNA in serum and detect YMDD (thyrosine, methionine, aspartate, aspartate) motif mutations in the same run. The assay was based on real-time polymerase chain reaction (Rt-PCR) with YMDD-specific hybridization probes. Determination of YMDD motif was done by melting temperature analysis. External standard curve was used for quantifying viral DNA, which was generated by standard sera (VQC S2220) including HBV-DNA between concentrations of 1000 to 3 million copies/ml. The assay was compared with commercial quantitative kit (Artus HBV RG PCR; Qiagen, Germany), commercial line prob assay (INNO-LiPA HBV DR v1.0; Innogenetics, Belgium) and direct DNA sequencing method. Thirty-eight serum samples obtained from 20 chronic hepatitis B patients (7 female, 13 male; age range: 27-70 years) treated with only lamivudine and were negative for HIV and HCV antigen and antibodies were tested in the study. The analytical sensitivity of the assay was found as 200 copies/ml, with a dynamic range of 1 x 103 to 3 x 107 copies/ml. PCR efficiency of the in-house assay was found to be 1.98. Comparison of log10 HBV-DNA concentrations determined by the in-house and commercial quantitative kits showed a significant correlation (r= 0.681). Melting temperature (Tm) analysis was used for the YMDD motif determination and found to be 59.86°C for YMDD, 56.34°C for YVDD and 55.10°C for YIDD. The results of the in-house assay, DNA sequencing and LiPA were concordant in samples with homogeneous virus population, and in-house assay could also detect the major type of YMDD motif in mixed viral populations The Rt-PCR method which was developed in this study is a rapid, accurate and reproducible method for quantifying HBV-DNA and detecting the predominant YMDD motif in the same run in two hours duration. It was concluded that this method may be a convenient tool for monitoring HBV-infected patients receiving lamivudine treatment.
Key words: Hepatitis B virus; HBV-DNA; lamivudine; resistance; mutation; YMDD; real-time PCR.
Geliş Tarihi (Received): 03.05.2011 • Kabul Ediliş Tarihi (Accepted): 27.06.2011
GİRİŞ
Hepatit B virusu (HBV) hepatotropik DNA virusu olup, kronik enfeksiyona yol açar. Dünya genelinde yaklaşık 350 milyon kişi HBV ile kronik olarak enfektedir1,2. Kronik HBV enfeksiyonu persistan karaciğer enfeksiyonuna neden olarak bir ömür boyu sürebilir. Günümüzde kronik hepatit B tedavisinde interferon-alfa (IFN-a) ve nükleotid analogları kullanılmaktadır. Lamivudin ve adefovir ile ilgili çok sayıda veri mevcut olup, entekavir, telbivudin ve tenofovir kullanıma giren diğer ilaçlardır3.
Lamivudin {(-) 2’,3’-dideoksi-3’-thiasitidin} zincir sonlandırıcı özelliği ile HBV-DNA replikasyonunu inhibe eder4. Lamivudin güvenilir, etkin ve pahalı olmayan bir ilaç olmasına karşın, viral yükteki artış ve serum alanin aminotransferaz (ALT) düzeyindeki artışla birlikte ortaya çıkan ilaç direnci önemli bir sorundur. Viral polimeraz bölgesindeki YMDD motifinde bulunan ikinci aminoasitteki (rtM204V/I/S) mutasyon lamivudin direncine neden olmaktadır5-7. Tam olarak viral süpresyonun sağlanamadığı veya direnç gelişen hastalarda, lamivudin ya bir başka ilaçla değiştirilmeli ya da farklı bir nükleotid analoğu ile kombine edilmelidir3,8. Viral süpresyon HBV-DNA düzeyi ile takip edilir. Genotipik yöntemler ve viral DNA takibi direnç gelişimini takip etmede kullanılan yöntemlerdir. HBV-DNA düzeyindeki bir logaritma (log) artış, dirençli mutantların ortaya çıktığının göstergesidir. Sıklıkla kullanılan genotipik yöntemler ise dizi analizi, LiPA (line prob assay) ve restriksiyon enzim analizidir (REA)9. Tedavi takibinde iki farklı yöntemin kullanılması (viral DNA düzeyi belirlenmesi ve genotipik direnç tayini) maliyeti artırmakta, yoğun iş yükü gerektirmekte ve uzun zaman almaktadır. Bu çalışmada, HBV-DNA düzeyi ve eş zamanlı olarak YMDD motif mutasyonunu saptayabilecek gerçek zamanlı polimeraz zincir reaksiyonu (Rt-PCR) testinin geliştirilmesi amaçlanmış ve bu yöntemin lamivudin alan hastalarda tedavi takibi ve ilaç değişimine karar vermede yardımcı olması hedeflenmiştir.
GEREÇ ve YÖNTEM
Hastalar ve Klinik Örnekler
Bu çalışmada tek başına lamivudin tedavisi almakta olan 20 kronik hepatit B hastasına (7 kadın, 13 erkek; yaş aralığı: 27-70 yıl, ortanca yaş: 50 yıl) ait 38 serum örneği kullanıldı. Hastalardan altısı HBeAg pozitif iken, kalan 14’ü negatif bulundu. Hastaların tamamının genotip D ile enfekte olduğu S gen bölgesinden yapılan dizi analizi ile belirlendi. Tüm hastaların anti-HCV, anti-HDV ve anti-HIV1/2 testleri negatif idi. Serum örnekleri lamivudin tedavisinin başlangıcından 2-32 hafta içerisinde alınarak alikotlandı ve kullanılıncaya kadar -80°C’de saklandı. Hastaların her birinden 1-3 arasında serum örneği alındı.
Viral DNA Ekstraksiyonu
Viral DNA 200 µl serum örneğinden üretici firma önerileri doğrultusunda “High Pure Viral Nucleic Acid Kit” (Roche Applied Science, Mannheim, Almanya) kullanılarak gerçekleştirildi. Saflaştırılmış serum ekstraktları LiPA testi, dizi analizi ve geliştirilen Rt-PCR testinde kullanıldı.
LiPA Testi (INNO-LİPA HBV DR)
Üretici firma önerileri doğrultusunda INNO-LiPA HBV DR v1.0 testi (Innogenetics, Belçika) kullanılarak YMDD motif mutasyonu analizi yapıldı.
Dizi Analizi
HBV genomunun polimeraz gen bölgesi PCR ile çoğaltıldı. Seçilmiş primerler olarak; öncül primer; 5’-CCCTGCTCGTGTTACAGGCGG-3’ (188-208. nükleotidler), revers primer; 5’-GTTGCGTCAGCAAACACTTGGCA-3’ (1176-1198. nükleotidler) kullanıldı. 50 µl’den oluşan PCR karışımı içerisinde 10 µl DNA ekstraktı, 0.2 mM dNTP, 0.5 mM MgCl2, 20 pmol öncül ve revers primer, 1.5 U Taq DNA polimeraz (Hot Start Taq DNA polymerase, Fermentas, Vilnius, Litvanya) ve 5 µl 10x Taq bulunmaktaydı. PCR, 94°C’de denatürasyon sonrası, 54°C’de 1 dakika, 72°C’de 2 dakikadan oluşan 35 siklustan oluşuyordu. Ürünler, etidyum bromür ile boyandıktan sonra %2’lik agaroz jel elektroforezi ile tespit edildi. Amplikonlar ticari kit ile (High Pure PCR Product Purification Kit; Roche Applied Science) saflaştırıldı. PCR ürünlerinin dizi analizi, her iki dizi için ayrı ayrı gerçekleştirildi (Macrogen Inc. Seul, Kore). Mutasyonlar referans HBV-DNA dizileri ile karşılaştırılarak tespit edildi.
Serum HBV-DNA Kantitasyonu
Viral DNA miktarı, ticari bir Rt-PCR kiti ile (Artus HBV RG PCR kit, Qiagen Inc., Hamburg, Almanya) üretici firma önerileri doğrultusunda tayin edildi. 200 µl plazmadan ticari kit (Qiagen Inc., Hamburg, Almanya) ile ekstrakte edilen DNA kullanıldı.
Geliştirilen Eş Zamanlı HBV-DNA Analizi ve YMDD Motif Mutasyonu Analizi Testi
Polimeraz gen bölgesinde 680 ile 783. nükleotidler arasında yer alan ve Cane ve arkadaşları10 tarafından tanımlanan PCR primerleri (5’-TACTAGTGCCATTTGTTCAGTGG-3’ ve 5’-CACGATGCTGTACAGACTTGG-3’) kullanıldı. Bu yöntemde Cy5 ve FAM ile işaretli hibridizasyon probları ile Cane10 tarafından tarif edilen üç probdan sadece YMDD motifi için belirlenen prob kullanıldı (Tablo 1). Primer ve prob dizileri GenBank’tan elde edilen farklı HBV genotipleri ile karşılaştırılarak kontrol edildi. (Şekil 2)
HBV-DNA kantitasyonu için, 1000 ile 3 milyon kopya/ml arasında viral DNA içeren beş farklı serum örneğinden oluşan VQC S2220 paneli (güncel adıyla Acrometriks, ABD) kullanıldı. Her çalışmada paneldeki beş farklı serum örneği de kantitasyonu belirlemek amacıyla kullanıldı.
PCR, cam kapillerler içerisinde LightCycler 2.0 (Roche Diagnostics) cihazında gerçekleştirildi. Reaksiyon parametreleri üretici firma önerilerine göre belirlendi. En uygun konsantrasyonun tespitinde, en yüksek floresansın tespit edildiği en düşük siklus (Ct) belirlendi. Amplifikasyon için 2x premiks Taq (2mM MgCl2) içeren 25 µl’lik reaksiyon karışımı kullanıldı. Her bir prob ve primerden 8 pmol ve 5 µl ekstrakte edilmiş DNA, reaksiyon karışımına dahil edildi. PCR programı; 95°C’de 10 saniyelik işlem sonrasında, 95°C’de 3 saniye, 50°C’de 10 saniye, 72°C’de 10 saniyeden oluşan 45 siklusluk program olarak belirlendi. Hasta serumlarının tamamından yapılan izolasyon ve amplifikasyon çalışmaları tekrar edilerek ikili çalışıldı.
YMDD motif mutasyonu tespitinde erime noktası sıcaklığı analizi kullanıldı. Bu yöntemde PCR sonrası elde edilen ürün önce 95°C’ye kadar ısıtıldı, ardından hızlıca 40°C’ye soğutuldu ve sonra yeniden 95°C’ye ısıtıldıktan sonra saniyede 0.2°C’lik ısı azaltımı esnasında 670 nm dalga boyunda elde edilen floresansdaki değişim incelendi. Vahşi tip ve mutant türlerinin tayininde YMDD, YVDD ve YIDD içeren HBV-DNA’nın klonlanlanmış gen fragmanları kullanıldı. Klonlanmış gen fragmanları 104 kopya/ml konsantrasyonda idi.
Geliştirilen yöntemde mutant ve vahşi tip HBV-DNA içeren karışımların saptama sınırını tespit edebilmek için, YMDD’nin yanı sıra, YVDD veya YIDD’den yüzde 0, 10, 25, 50, 75, 90 ve 100 oranında içeren örnekler hazırlandı.
Klonlanmış HBV-DNA Gen Fragmanları
YMDD bölgesinde farklılık gösteren (YMDD, YVDD ve YIDD) klonlanmış HBV-DNA gen fragmanları, H. G. Niesters ve S. Pas (Erasmus Tıp Merkezi, Hollanda) tarafından sağlandı.
İstatistiksel Analiz
Bu amaçla SPSS (versiyon 11) programı kullanıldı ve p< 0.05 değerleri anlamlı kabul edildi.
BULGULAR
Duyarlılık ve Özgüllük Analizi
Analitik duyarlılık sınırının tespitinde ve eksternal kantitasyon eğrisinin oluşturulmasında VQC referans paneli kullanılmış ve yöntemin analitik duyarlılık sınırı 200 kopya/ml, dinamik aralığının ise 1 x 103-3 x 107 kopya/ml olduğu tespit edilmiştir. Geliştirilen yöntemin özgüllüğünün tespitinde 20 farklı kişiden alınmış, HBsAg, anti-HBc ve HBV-DNA negatif serum örneği incelenmiş ve hiçbir örnekte yalancı pozitiflik saptanmamıştır.
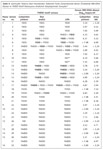
Test içi ve testler arası değişkenlik analizinde VQC panel örnekleri kullanılmış, her bir serum örneği üç farklı günde üçer kez çalışılmıştır. Ortalama Ct değerleri, belirsizlik katsayısı (CV) ve teste giren HBV-DNA miktarları Tablo 1’de gösterilmiştir.
Test içi (ortalama 1.02) ve testler arasında (ortalama 1.02) (p= 0.900) yapılan belirsizlik analizinde istatistiksel açıdan anlamlı bir fark tespit edilmemiştir.
Klonlanmış HBV-DNA fragmanlarından YMDD, YVDD ve YIDD için ayrı ayrı erime noktası sıcaklığı analizi gerçekleştirilmiş ve bu değerler sırasıyla 59.86 ± 1.77°C, 56.34 ± 0.34°C ve 55.10 ± 0.31°C olarak belirlenmiştir (Şekil 3)
Vahşi ve mutant tip virusların tespitindeki duyarlılık oranı ise %50/50 olarak saptanmıştır.
Gerçek Zamanlı PCR (Rt-PCR) ile Elde Edilen Kantitasyon Değerlerinin Doğruluğu
Rt-PCR ile elde edilen kantitasyon değerlerinin doğruluğunun belirlenebilmesi için HBV-DNA içermeyen ve 1 x 103 ile 3 x 107 kopya/ml HBV-DNA içeren VQC paneli kullanılmış ve geliştirilen yöntemle elde edilen log10 HBV-DNA değerleri, beklenen değerler ile yüksek korelasyon göstermiştir. Şekil 4 PCR etkinliği ise 1.98 olarak bulunmuştur.
Viral Yük ve YMDD Motif Mutasyonu Sonuçlarının Karşılaştırılması
Geliştirilen yöntemle elde edilen HBV-DNA düzeyi ve YMDD motif mutasyonu analizi sonuçları ticari bir kit olan Artus HBV RG PCR kit (Qiagen Inc.), LiPA ve dizi analizi sonuçlarıyla karşılaştırılmıştır (Tablo 2)
Toplam 18 hastadan elde edilen 38 serum ile yapılan çalışmalarda, geliştirilen yöntem ve ticari Artus kitinin sonuçlarından 18’i her iki yöntemde de dinamik aralık içerisinde bulunmuştur. Örnek sayısı az olmasına karşın her iki yöntemle elde edilen sonuçların log10 HBV-DNA korelasyonu incelenmiş ve sonuçların birbirine yakın olduğu tespit edilmiştir (r= 0.681, p= 0.002) (Şekil 5). Geliştirilen yöntemle elde edilen HBV-DNA düzeyi genellikle ticari Artus kitine oranla daha yüksek izlenmiştir. Testler arasında ortalama fark 0.54-1.06 (0.19-2.09) log10 kopya/ml olarak bulunmuştur. İki yöntemle yapılan test sonuçları karşılaştırıldığında; testlerin %27’si (5 serum) 0.5 log10‘dan daha az fark gösterirken, %55’inde (10 serum) 0.5-1 log10 kopya/ml fark tespit edilmiştir.
Geliştirilen yöntemde YMDD motif analizi 38 örnekten 36’sında yapılmış, diğer iki örnekte ise HBV-DNA düzeyi 1000 kopya/ml’nin altında olduğu için analiz yapılamamıştır. LiPA’da birden fazla bant varsa, koyu renkli olan bant; dizi analizinde ise birden fazla aminoasit varsa aminoasit belirteci yüksek olan baskın tip olarak belirlenmiştir. Geliştirilen yöntem YMDD motif mutasyon analizi açısından dizi analizi ve LiPA ile karşılaştırıldığında, karışık örneklerde baskın olan tipin tespit edilebildiği görülmüştür. Tek tip viral popülasyon varlığında üç yöntemle elde edilen sonuçlar tam olarak birbiriyle uyumlu bulunmuştur. Serum örneklerinden 8’inde (serum no: 5-7, 12-13, 15, 17, 19) dizi analizi ve LiPA ile birbirleriyle uyumlu olarak karışık popülasyon varlığı saptanmasına karşın, bu örneklerin altısında geliştirilen yöntemle baskın olan tip, ikisinde ise (serum no: 6 ve 7) baskın olmayan tip viral popülasyon saptanmıştır.
Dört numaralı hastaya ait örneklerde LiPA ile 204 numaralı aminoasit pozisyonunda herhangi bir sonuç elde edilememiştir. Hastanın dizi analizi sonuçları incelendiğinde, rtM204I mutasyonunun (YIDD) yanı sıra 201. kodonda LiPA ile hibridizasyon probu oluşumunu engelleyen ilave bir mutasyon daha olduğu tespit edilmiş ve bu durum üretici firmaya da aktarılmıştır.
TARTIŞMA
Lamivudin kronik HBV tedavisinde yaygın olarak kullanılan bir ilaçtır. Viral polimeraz geninde bulunan YMDD motifinde görülen mutasyon nedeniyle tedavi takibinde YMDD motif mutasyonu analizi ve viral yük tayini önem taşır. Tedaviden önceki viral yük ve tedavi süresi, mutasyon gelişimini etkilemektedir. Tedavi süresinin beş yıla uzadığı olgularda mutasyon oranı %60-70’e varabilmektedir11. Antiviral direnç gelişiminde önce dirençle ilgili mutantlar saptanırken, bunu viral yük artışı ve ALT düzeyindeki artış takip eder11,12.
Bu çalışmada geliştirdiğimiz yöntem, HBV-DNA düzeyi tayini ve eş zamanlı olarak YMDD motif mutasyonu analizini hızlı ve pahalı olmayan bir şekilde gerçekleştirebilmektedir. Bu yöntemde YMDD mutasyonu analizi için erime noktası sıcaklığı (Tm) analizine dayalı YMDD motifine özgü hibridizasyon probları kullanılmıştır. Problar yüksek düzeyde korunmuş olan bir bölgeden seçildiği için farklı HBV genotiplerinde de kullanılabilir; ancak bu çalışmada sadece genotip D’nin bulunması nedeniyle, konu ile ilgili daha ileri çalışmaların yapılması gerektiği düşünülmüştür. Tm analizi ile mutant virusların (YIDD veya YVDD) vahşi tipten daha düşük erime noktası sıcaklığı gösterdikleri, ayrıca mutant virusların da kendi aralarında farklı Tm değerleriyle birbirinden ayırt edilebildikleri saptanmıştır. Geliştirilen yöntemle, karışık viral popülasyonlarda baskın olan tipin tespit edildiği de izlenmiştir. Bu yöntem, dizi analizi ile benzer şekilde üç serum örneğinde (serum no: 4, 8, 14) eş sonuçlar vermesine karşın, bu üç örnekte LiPA ile karışık viral popülasyon varlığı saptanmıştır. LiPA’nın özellikle karışık viral popülasyon varlığında yakalama alt sınırı %10’luk değer ile ön plana çıkmakta olup, dizi analizinde %30 olan bu oran, geliştirdiğimiz yöntemde %50 olarak belirlenmiştir12,13. Ancak LiPA testinde mutasyon saptamada alt sınırın düşük olmasına karşın, LiPA şeridi üzerinde bulunmayan mutasyonların tespit edilmesi mümkün değildir. Bu nedenle 4 numaralı hastaya ait örneklerde YMDD motifi dışında bir başka bölgede görülen mutasyon, hibridizasyonu engelleyerek testin sonuç vermesini engellemiştir. Bu durum üretici firmaya iletilmiş ve yeni kuşak testin çıkarılmasıyla düzeltilmiştir.
Lamivudin tedavisi alan hastalarda HBV-DNA düzeylerinin düşmesi, analitik duyarlılık sınırının önemini artırmaktadır14. Geliştirilen yöntemin analitik duyarlılık sınırı 200 kopya/ml (yaklaşık 40 IU/ml), dinamik aralığı ise 103 ile 107 kopya/ml olarak tespit edilmiştir. Geliştirilen yöntem ve ticari Artus kiti ile elde edilen HBV-DNA düzeyleri karşılaştırıldığında, örnekler arasında anlamlı bir korelasyon olmasına karşın, örneklerin yaklaşık yarısında 1 log10 kopya/ml’den fazla fark olduğu belirlenmiştir. Bu farklılığın DNA ekstraksiyon yöntemlerindeki farklılıktan ve ayrıca Artus kitinde kullanılan plazmidlerin ekstraksiyona dahil edilmemesinden kaynaklanabileceği düşünülmüştür. Ayrıca son dönemde Artus HBV-DNA testi tekrar kalibre edilmiş ve elde edilen sonuçların iki ile çarpıldığı öğrenilmiştir. Geliştirilen yöntemin en önemli dezavantajı ise iç kalite kontrolünün yapılmamasıdır. Bu durum yalancı negatifliklere yol açabilecek olmasına karşın, çalışmamızda yalancı negatifliğe rastlanmamıştır.
Çeşitli araştırıcılar tarafından YMDD motif mutasyon analizi ya da HBV-DNA düzeyi tayini için birçok Rt-PCR çalışması yapılmıştır10,15-20. Ancak bu iki parametreyi eş zamanlı olarak Rt-PCR yöntemiyle gerçekleştirmeye yönelik az sayıda çalışma mevcuttur21-23. Geliştirilen yöntemin klinik uygulamada en önemli avantajı, HBV-DNA düzeyini belirleyebilmesinin yanı sıra aynı testte eş zamanlı olarak baskın olan YMDD motif analizini de kısa sürede gerçekleştirebilmesidir. Tedavide kullanılan antiviral ajanın değişimi için genellikle viral yükün tedavi esnasında 10 kat artması karar verdirici olmaktadır11. Bu nedenle viral yük tayini ve baskın viral popülasyonun aynı testte eş zamanlı olarak ve kısa sürede saptanması tedavi takibini kolaylaştıracaktır. Sonuç olarak bu çalışmada geliştirilen Rt-PCR testi, HBV-DNA düzeyi ve YMDD motif mutasyonu analizini tek bir çalışmada ve iki saat süre içerisinde gerçekleştirebilen ekonomik bir yöntem olup, lamivudin tedavisi alan kronik HBV hastalarında tedavi takibinde alternatif olarak kullanılabilir.
TEŞEKKÜR
Bu çalışmada kullanılan plazmidleri temin eden S. Pas ve H.G. Niesters’e (Erasmus Tıp Merkezi, Viroloji Bilim Dalı, Hollanda) teşekkür ederiz.
KAYNAKLAR
- Lee WM. Hepatitis B virus infection. N Engl J Med 1997; 337(24): 1733-45.
- Hilleman MR. Critical overview and outlook: pathogenesis, prevention, and treatment of hepatitis and hepatocarcinoma caused by hepatitis B virus. Vaccine 2003; 21(32): 4626-49. [Özet]
- Nguyen MH, Keeffe EB. Chronic hepatitis B: early viral suppression and long-term outcomes of therapy with oral nucleos(t)ides. J Viral Hepat 2009; 16(3): 149-55. [Özet]
- Fischer KP, Gutfreund KS, Tyrrell DL. Lamivudine resitance in hepatitis B: mechanisms and clinical implications. Drug Resist Updat 2001; 4(2): 118-28. [Özet]
- Stuvyer LJ, Locarnini SA, Lok A, et al. Nomenclature for antiviral resistant human hepatitis B mutations in the polymerase region. Hepatology 2001; 33(3): 751-7. [Özet]
- Niesters HG, De Man RA, Pas SD, Fries E, Osterhaus AD. Identification of a new variant in the YMDD motif of the hepatitis B virus polymerase gene selected during lamivudine therapy. J Med Microbiol 2002; 51(8): 695-9. [Özet] [PDF]
- Bozdayi AM, Uzunalimoglu O, Turkyilmaz AR, et al. YSDD: a novel mutation in HBV DNA polymerase confers clinical resistance to lamivudine. J Viral Hepat 2003; 10(4): 256-65. [Özet]
- Dan YY, Wai CT, Lee YM, Sutedja DS, Seet BL, Lim SG. Outcome of lamivudine-resistant hepatitis B virus is generally benign except in cirrhotics. World J Gastroenterol 2005; 11(28): 4344-50. [Özet]
- Sablon E, Shapiro F. Advances in molecular diagnosis of HBV infection and drug resistance. Int J Med Sci 2005; 2(1): 8-16. [Özet] [Tam Metin] [PDF]
- Cane PA, Cook P, Ratcliffe D, Mutimer D, Pillay D. Use of real-time PCR and fluorimetry to detect lamivudine resistance associated mutations in hepatitis B virus. Antimicrob Agents Chemother 1999; 43(7): 1600-8. [Özet] [Tam Metin] [PDF]
- Lok AS, McMahon BJ. Chronic hepatitis B. Hepatology 2007; 45(2): 507-39.
- Pas SD, de Man RA, Fries E, Osterhaus AD, Niesters HG. The dynamics in the YMDD motif of the hepatitis B virus polymerase gene during and after lamivudine treatment as determined by reverse hybridisation. J Clin Virol 2002; 25(1): 63-71. [Özet]
- Aberle SW, Kletzmayr J, Watschinger B, Schmied B, Vetter N, Puchhammer-Stockl E. Comparison of sequence analysis and the INNO-LiPA HBV DR line probe assay for detection of lamivudine resistant hepatitis B virus strains in patients under various clinical conditions. J Clin Microbiol 2001; 39(5): 1972-4. [Özet] [Tam Metin] [PDF]
- Hatzakis A, Magiorkinis E, Haida C. HBV virological assessment. J Hepatol 2006; 44(Suppl 1): S71-6. [Özet]
- Whalley SA, Brown D, Teo CG, Dusheiko GM, Saunders NA. Monitoring the emergence of hepatitis B virus polymerase gene variants during lamivudine therapy using the LightCycler. J Clin Microbiol 2001; 39(4): 1456-9. [Özet] [Tam Metin] [PDF]
- Chieochansin T, Chutinimitkul S, Payungporn S, et al. Rapid detection of lamivudine-resistant hepatitis B virus mutations by PCR based methods. Tohoku J Exp Med 2006; 210(1): 67-78. [Özet]
- Wang RS, Zhang H, Zhu YF, Han B, Yang ZJ. Detection of YMDD mutants using universal template real-time PCR. World J Gastroenterol 2006; 12(8): 1308-11. [Özet]
- Pas Sdi Fries E, De Man RA, Osterhaus AD, Niesters HG. Development of a quantitative real-time detection assay for hepatitis B virus DNA and comparison with two commercial assays. J Clin Microbiol 2000; 38: 2897-901. [Özet] [Tam Metin] [PDF]
- Allice T, Cerutti F, Pittaluga F, et al. COBAS AmpliPrep-COBAS TaqMan hepatitis B virus (HBV) test: a novel automated real-time PCR assay for quantification of HBV DNA in plasma. J Clin Microbiol 2007; 45(3): 828-34. [Özet] [Tam Metin] [PDF]
- Liu Y, Hussain M, Wong S, Fung SK, Yim HJ, Lok AS. A genotype-independent real-time PCR assay for quantification of hepatitis B virus DNA. J Clin Microbiol 2007; 45(2): 553-8. [Özet] [Tam Metin] [PDF]
- Punia P, Cane P, Teo CG, Saunders P. Quantitation of hepatitis B lamivudine resistant mutants by real-time amplification refractory mutation system PCR. J Hepatol 2004; 40(6): 986-92. [Özet]
- Wightman F, Walters T, Ayres A, et al. Comparison of sequence analysis and a novel discriminatory real-time PCR assay for detection and quantification of lamivudine-resistant hepatitis B virus strains. J Clin Microbiol 2004; 42(8): 3809-12. [Özet] [Tam Metin] [PDF]
- Pas SD, Noppornpanth S, van der Eijk AA, de Man RA, Niesters HG. Quantification of the newly detected lamivudine resistant YSDD variants of hepatitis B virus using molecular beacons. J Clin Virol 2005; 32(2): 166-72. [Özet]
İletişim (Correspondence):
Uzm. Dr. Harun Ağca
Tavşanlı Doç. Dr. Mustafa Kalemli Tavşanlı Devlet Hastanesi,
B Blok, Tavşanlı, Kütahya, Türkiye.
Tel: +90 505 844 3004,
E-posta: drharunagca@yahoo.com