Candidaİzolatlarının Antifungal Duyarlılığının Belirlenmesinde
Klinik Laboratuvar Standartları Enstit�s� (CLSI) ve
Avrupa Antimikrobiyal Duyarlılık Testleri Komitesi (EUCAST)
Sıvı Mikrodil�syon Y�ntemlerinin Karşılaştırılması*
Comparison of Clinical Laboratory Standards Institute (CLSI) and
European Committee on Antimicrobial Susceptibility Testing (EUCAST)
Broth Microdilution Methods for Determining the Susceptibilities of Candida isolates
Burcu DALYAN CİLO1, Tuncay TOPA�1, Harun AĞCA1, Sezcan SAĞLAM1, Kadir EFE1, Beyza ENER1
1 Uludağ �niversitesi Tıp Fak�ltesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Bursa.
1 Uludağ University Faculty of Medicine, Department of Medical Microbiology, Bursa, Turkey.
* Bu �alışma, Uludağ �niversitesi Bilimsel Araştırma Projeleri Birimi tarafından KUAP (T)-2014/3 no'lu proje ile desteklenmiştir.
�Z
Candida t�rleri y�ksek mortalite ve morbiditeyle ilişkili kan dolaşımı enfeksiyonlarına sebep olan ilk 10 etken arasındadır. Bir�ok yeni antifungal ilacın geliştirilmesine rağmen epidemiyolojik �alışmalar Candida izolatlarındaki antifungal direncin ciddi bir problem haline gelmeye başladığını g�stermiştir. Antifungal duyarlılığı �l�mek i�in iki standart y�ntem vardır ve bu �alışmada kandan elde edilen Candida izolatlarının amfoterisin B, flukonazol, itrakonazol, vorikonazol, posakonazol ve anidulofungin duyarlılığını belirlemek i�in "Clinical and Laboratory Standards Institute (CLSI)" ve "European Committee on Antimicrobial Susceptibility Testing (EUCAST)" sıvı mikrodil�syon y�ntemlerinin karşılaştırılması ama�lanmıştır. �alışmada 74 Candida albicans, 67 Candida parapsilosis, 30 Candida glabrata ve 18 Candida tropicalis izolatı kullanılmıştır. Anidulofungin hari�, minimum inhibit�r konsantrasyon değerleri, CLSI y�nteminde 24 ve 48 saat ink�basyondan sonra, EUCAST y�nteminde sadece 24 saat ink�basyondan sonra belirlenmiştir. Her iki y�ntemle elde edilen MİK değerleri � 2 dil�syon sınırları i�erisinde ise uyumlu olarak kabul edilmiştir. Her antifungal i�in y�ntemler arasındaki kategori uyumunda klinik sınır değerler ve epidemiyolojik eşik değerlerden yararlanılmıştır. Y�ntemler arasındaki uyum (� 2 dil�syonda) t�r, ila� ve ink�basyon zamanına bağımlı olarak bulunmuştur. Yirmi d�rt saat ink�basyon sonunda amfoterisin B, itrakonazol, posakonazol ve anidulofunginde iyi (> %90) kategorisinde uyum bulunurken, flukonazol ve vorikonazolde, �zellikle nispeten daha yavaş �reyen C.glabrata ve C.parapsilosis izolatlarında daha d�ş�k kategorisinde uyum (< %85) bulunmuştur. M�kemmel kategori uyumu (%100) amfoterisin B/C.parapsilosis, C.glabrata, C.tropicalis ve andilofungin/C.albicans, C.glabrata, C.tropicalis ile g�r�l�rken en k�t� uyum, posakonazol ve C.albicans (24 saate %71.6; 48 saatte %73) arasında saptanmıştır. Tedavide sık kullanılan ila�lar olan flukonazol ve anidulafungine her iki y�ntemle tespit edilen diren� C.albicans (sırasıyla %1.3; %2.7), C.glabrata (sırasıyla 0%, %3.3) ve C.tropicalis'de (sırasıyla 0%, %5.6), in vitro azalmış duyarlılık C.parapsilosis ve flukonazolde (24 saatte %11.9; 48 saatte %17.9) g�r�lm�şt�r. Flukonazol ve vorikonazol arasında �apraz diren� �� C.parapsilosis izolatında saptanmış ve bir C.albicans izolatında ise �ok ilaca diren� (flukonazol, itrakonazol, posakonazol ve anidulafungin) tespit edilmiştir. �alışma sonucunda, her iki y�ntemin benzer olduğu ve laboratuvarların tercihine g�re kullanılabileceği g�zlenmiştir. CLSI antifungal duyarlılık sonu�larının 24 saat ink�basyon sonunda değerlendirilebileceğinin ancak bazen, C.glabrata gibi yavaş �reyen t�rlerde 48 saat ink�basyon sonucunda değerlendirme yapılması gerektiğinin �nemli olduğu saptanmıştır.
Anahtar s�zc�kler: Candida t�rleri; antifungal duyarlılık; minimum inhibit�r konsantrasyon.
ABSTRACT
Candida species are among the top 10 pathogens causing bloodstream infections associated with high morbidity, mortality. In spite of the development of new antifungal drugs, epidemiological studies have shown that resistance to antifungal drugs among Candida isolates is becoming a serious problem. The aim of this study was to compare the antifungal broth microdilution methods of the Clinical and Laboratory Standards Institute (CLSI) and European Committee on Antimicrobial Susceptibility Testing (EUCAST) for amphotericin B, fluconazole, itraconazole, voriconazole, posaconazole and anidulafungin susceptibility of Candida blood isolates. The study consisted of 74 Candida albicans, 67 Candida parapsilosis, 30 Candida glabrata, and 18 Candida tropicalis isolates. The minimum inhibitory concentrations were determined after 24 and 48 hour of incubation with CLSI method and only 24 hour of incubation with EUCAST method except anidulofungin. The MIC values obtained by both methods were considered to be compatible within � 2 dilution limits. The categorical agreement between methods for each antifungal agent was assessed using clinical break points and epidemiological cut-off values. The agreement (� 2 dilution) between the methods was found to be species, drug, and incubation time dependent. After 24 hour incubation, good agreement category (> 90%) was detected between amphotericin B, itraconazole, posaconazole and anidulofungin, but was lower category (< 85%) was determined with fluconazole and voriconazole especially for relatively slow growing C.glabrata and C.parapsilosis isolates. Excellent categorical agreement (100%) was observed for amfoterisin B/C.parapsilosis, C.glabrata, C.tropicalis and anidulofungin/C.albicans, C.glabrata, C.tropicalis but least category was determined for posaconazole and C.albicans (71.6% at 24 hour; 73% at 48 hour). In vitro resistance of therapeutically used fluconazole and anidulafungin determined by both methods was rare among C.albicans (1.3%, 2.7% respectively), C.glabrata (0%, 3.3% respectively) and C.tropicalis (0%, 5.6% respectively) isolates but, an increase of non-susceptible isolates were observed among C.parapsilosis (11.9% at 24 hour of incubation; 17.9% at 48 hour of incubation) for fluconazole. There was also a cross resistance between fluconazole and voriconazole for three C.parapsilosis isolates and one multidrug resistant (fluconazole, itraconazole, posaconazole and anidulofungin) C.albicans isolate (fluconazole, itraconazole, posaconazole and anidulofungin). As a result in this study, it was determined thatboth methods were similar and can be used according to preference of laboratories. The CLSI antifungal susceptibility test results can be assessed at the end of 24 hour incubation, but sometimes it is important that the evaluation should be performed as a result of 48 hour incubation in slow growing species such as C.glabrata.
Keywords: Candida species; antifungal susceptibility; minimum inhibitory concentration.
Geliş Tarihi (Received): 21.07.2017 - Kabul Ediliş Tarihi (Accepted): 08.11.2017
GİRİŞ
İnvaziv mantar enfeksiyonları sıklıkla ağır seyirli, hızlı ilerleyen, tanısı zor ve tedaviye diren�li hastalıklar olup en sık karşılaşılan etkenler Candida ve Aspergillus t�rleridir. G�n�m�zde geniş spektrumlu antibiyotiklerin ve imm�ns�presif ila�ların yaygın kullanımı, sitotoksik tedaviye bağlı uzun s�ren n�tropeniler, artan kateter kullanımı ve artan maj�r kardiyak ve abdominal cerrahi gibi girişimsel işlemler nedeniyle Candida t�rleri fırsat�ı hastane enfeksiyonu etkenleri arasında �n sıralarda yer almaktadırlar1. İnvaziv Candida enfeksiyonlarında erken tanı ve tedavi mortalite ve morbiditenin azaltılması a�ısından �nemlidir. Son yıllarda tedavide kullanılabilecek farklı etki mekanizmalarına sahip yeni antifungal ila�ların geliştirilmesi ve artan antifungal diren� nedeniyle antifungal duyarlılık testlerine olan gereksinim artmış ve geliştirilen y�ntemler sayesinde antifungal duyarlılık testleri klinik laboratuvarlarda daha fazla kullanılmaya başlanmıştır2,3.
Antibakteriyel duyarlılık testleri i�in standart y�ntemler uzun yıllardır uygulanmakla birlikte, antifungal duyarlılık testlerinde standardizasyon nispeten daha yenidir. İlk kez 1982 yılında "Clinical and Laboratory Standards Institute (CLSI)" (�nceki adı ile National Committee for Clinical Laboratory Standards) tarafından antifungal duyarlılık testleri i�in bir alt komite kurulması ile s�re� başlamıştır. Uzun ve kompleks bir standardizasyon s�reci, �ok merkezli �alışma sonu�ları ve konsensus dok�manlarından (1992'de M27-P; 1995'te M27-T; 1997'de M27-A; 2002'de M27-A2) sonra yeni antifungaller eklenerek hazırlanan M27-A3 rehberi ve ek bilgi dok�manı, 2008 yıllında yayınlanmıştır4,5. Sıvı dil�syon y�ntemi ve 48 saat ink�basyon sonunda minimum inhibit�r konsantrasyon (MİK) belirlenmesinin anlatıldığı bu rehberde Candida t�rleri i�in genel klinik sınır değerler bulunmakla birlikte, t�re �zg� klinik sınır değerleri bulunmamaktadır. Daha sonraki yıllarda, CLSI antifungal �alışma grubu ve �eşitli araştırmacılar tarafından antifungal duyarlılık sonu�larının daha erken (24 saat) değerlendirilme validasyonu, direnci daha iyi g�steren epidemiyolojik eşik ve t�re �zg� klinik sınır değerlerinin oluşması sağlanmıştır6. Bu gelişmeler sonunda ek bilgi dok�manı (M27-S4) 2012 yılında yenilenmiştir7.
Bir diğer uluslararası sıvı mikrodil�syon y�ntemi ise "European Committee on Antimicrobial Susceptibility Testing (EUCAST)" tarafından 2002 yılından itibaren �eşitli versiyonlarla (2002'de Discussion document E.Dis. 7.1; 2008'de Definitive Document E.Def 7.1; 2012'de Definitive Document E.Def 7.2) yenilenen ve daha �ok Avrupa'da tercih edilen referans (E.Def 7.3) y�ntemdir8. İki referans y�ntem benzer olmakla birlikte, besiyeri i�eriği, inok�lum miktarı, ink�basyon zamanı ve değerlendirme a�ısından bazı farklılıklar bulunmaktadır. EUCAST kılavuzu son yıllarda antifungal duyarlılık sonu�larının daha erken ve daha objektif olarak değerlendirilmesi y�n�nde değişiklikler yapmıştır8.
�lkemizde uzunca bir s�redir antibiyotik duyarlılık testlerinde CLSI rehberi kullanılmakla birlikte, Sağlık Bakanlığı'nın da �nerileri ile EUCAST rehberine ge�iş başlatılmıştır. Bu ge�işin en �nemli nedeni �lkemizin Avrupa Birliği'ne giriş s�reci ve EUCAST dok�manlarına �cretsiz olarak web sitesinden (www.eucast.org) ulaşılabilmesidir. Antifungal duyarlılıkla ilgili hen�z belirlenmiş bir s�re� olmamakla birlikte, kısa bir s�re i�inde EUCAST rehberinde �nerilen antifungal duyarlılık y�nteminin kullanımının artacağı beklenmektedir. Bu �alışmada, hastanemizde kan �rneklerinden elde edilen Candida izolatlarının antifungal ila�lara olan duyarlılıklarının CLSI ve EUCAST rehberlerine dayalı y�ntemler ile belirlenerek karşılaştırılması ve her iki y�ntem ile elde edilen sonu�ların değerlendirilmesi ama�lanmıştır.
GERE� ve Y�NTEM
�alışmada kan �rneklerinden elde edilen ve �imlenme borusu, mısır unu-tween 80 besiyerindeki morfoloji ve API ID32 C (bioMerieux Marcy I'Etoile, Fransa) ile Candida albicans (n= 74), Candida parapsilosis (n= 67), Candida glabrata (n= 30), Candida tropicalis (n= 18) olarak tanımlanan 189 Candida izolatı kullanıldı. Uludağ �niversitesi Tıp Fak�ltesi Tıbbi Mikrobiyoloji Anabilim Dalı'na ait stoklarda -80C'de saklanan izolatlar, Sabouraud Dekstroz agara (SDA) iki kez pasajlanarak canlandırıldı ve saf k�lt�r elde edildi. Ayrıca, C.parapsilosis ATCC 22019 ve C.krusei ATCC 6258 suşları kalite kontrol� i�in her deneyde kullanıldı.
�alışma izolatları ve kalite kontrol suşlarının flukonazol (Sigma Aldrich, St Louis, MO, ABD), vorikonazol (Pfizer Central Research, New York, NY, ABD), itrakonazol (Sigma Aldrich, ABD), posakonazol (Sigma Aldrich, ABD), amfoterisin B (Amresco, OH, ABD) ve anidulafungine (Pfizer Central Research, ABD) in vitro duyarlılıkları CLSI M27-A3 ve EUCAST EDef 7.3 rehberlerinde �nerilen sıvı mikrodil�syon y�ntemleri ile belirlendi4,8.
CLSI �nerilerine g�re; antifungal ila�lar, %0.2 glikoz i�eren RPMI 1640 besiyerinde sulandırılarak U tabanlı mikrodil�syon plaklarına uygun konsantrasyonda dağıtıldı. İnok�lum s�spansiyonu son konsantrasyonu 0.5 x 103-2.5 x 103 h�cre/ml olacak şekilde ayarlandı ve değişik konsantrasyonlarda antifungal bulunan mikrodil�syon kuyucuklarına dağıtıldı. Plaklar 35C'de ink�be edildi. Anidulafungin hari� diğer ila�ların plakları g�rsel olarak 24 ve 48 saat sonra değerlendirildi. Anidulafungin plakları 24 saat sonra sadece g�rsel değerlendirildi. Amfoterisin B i�in kontrol kuyucuğuna g�re �remenin tam inhibe edildiği kuyucuk, diğer ila�lar i�in ise �remenin belirgin azaldığı kuyucuk MİK olarak belirlendi4.
EUCAST �nerilerine g�re, CLSI �nerilerinden farklı olarak d�z tabanlı mikrodil�syon plakları, %2 glikoz i�eren RPMI 1640 besiyeri ve daha y�ksek inok�lum (0.5 x 105-2.5 x 105 h�cre/ml) i�erecek şekilde hazırlandı. Plaklar 35C'de ink�be edildi ve MİK değerleri 24 saat sonra 530 nm absorbansta spektrofotometrik olarak belirlendi. Amfoterisin B i�in kontrol kuyucuğuna g�re �remenin %100 inhibe olduğu kuyucuk, diğer ila�lar i�in ise %50 azaldığı kuyucuk MİK olarak belirlendi8.
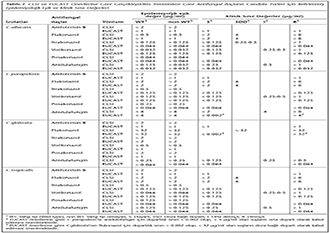
Her iki y�ntemle elde edilen MİK değerleri � 2 dil�syon sınırları i�erisinde ise, uyumlu olarak kabul edildi ve iki y�ntem arasında uyum oranı y�zde olarak hesaplandı. Kategori uyumunun belirlenmesinde, her iki y�ntem i�in kendi klinik sınır değerleri olduğu zaman klinik sınır değerlerinden, olmadığı zaman her iki y�ntemin kendi epidemiyolojik eşik değerlerinden (Tablo I) yararlanıldı6-8. CLSI ve EUCAST �nerileri ile belirlenen MİK değerleri ≤ eşik/duyarlı klinik sınır değerlerde veya > eşik/≥ diren�li klinik sınır değerlerde ise uyumlu kategori bulgusu olarak kabul edildi. CLSI �nerileri ile belirlenen MİK > eşik/≥ diren�li klinik sınır değer iken, EUCAST �nerileri ile belirlenen MİK ≤ eşik/duyarlı klinik sınır değer ise �ok b�y�k hata; CLSI �nerileri ile belirlenen MİK ≤ eşik/duyarlı klinik sınır değer iken, EUCAST �nerileri ile belirlenen MİK > eşik/≥ diren�li klinik sınır değerde ise b�y�k hata olarak değerlendirildi. CLSI �nerileri doğrultusunda ger�ekleştirilen y�ntem ile doza bağlı duyarlı/orta duyarlı olan suşlar, EUCAST �nerileri ile yapılan y�ntem ile duyarlı ya da diren�li olduğu zaman k���k hata olarak kabul edildi.
BULGULAR
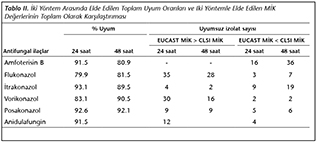
Tablo II'de iki y�ntem arasında 24 ve 48. saatlerde elde edilen toplam uyum oranları g�sterilmiştir. Tabloda da g�r�ld�ğ� gibi 24. saatte en d�ş�k uyum oranı (< %85) flukonazol ve vorikonazol i�in g�zlenmiştir. Amfoterisin B, itrakonazol, posakonazol ve anidulafungin i�in 24. saat uyum oranları > %90 olarak bulunmuştur. Amfoterisin B ve itrakonazol hari�, hem 24 hem de 48 saatlik ink�basyon sonunda uyumsuz izolatların �oğunda EUCAST �nerileri ile elde edilen MİK değerleri, CLSI �nerileri ile uygulanan y�ntemle bulunan MİK değerlerinden daha y�ksek saptanmıştır.
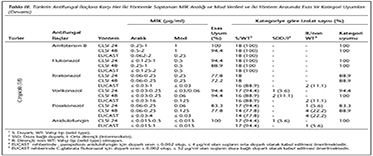
Tablo III'te t�rlerin antifungal ila�lara karşı her iki y�ntemle saptanan MİK aralığı, mod verileri ve iki y�ntem arasındaki esas ve kategori uyumları verilmiştir. En iyi esas uyum (%100) 24. saatte amfoterisin B/C.tropicalis ve anidulafungin/C.glabrata ve C.tropicalis i�in g�zlenmiştir. En k�t� uyum ise C.glabrata'nın 24. saatte elde edilen flukonazol ve vorikonazol sonu�larında tespit edilmiştir. Genel olarak 24. saatte g�zlenen uyum oranları daha iyi olmakla birlikte, C.glabrata ve C.parapsilosis izolatları i�in flukonazol ve vorikonazol a�ısından 48. saatte daha y�ksek uyum saptanmıştır. Kategori uyum değerlendirmesine g�re, amfoterisin B ve anidulafunginin �� t�rde %100 uyum g�sterdiği saptanmıştır. En k�t� (< %80) uyum ise C.albicans izolatlarında posakonazol i�in g�zlenmiştir (Tablo III).
CLSI �nerisine g�re uygulanan y�ntem ile amfoterisin B direnci hi�bir izolatta g�zlenmezken; EUCAST �nerilerine g�re uygulanan y�ntem ile diren�li olan bir C.albicans izolatı (non wild type; NWT) hari�, diğer t�m izolatlarda diren� saptanmamıştır. Flukonazolde doza bağlı duyarlılık (24 saat)/diren� (48 saat) C.albicans'da CLSI ile bir, EUCAST ile iki izolatta saptanmış ve iki y�ntemle de diren�li olarak saptanan izolat itrakonazol, posakonazol ve anidulafungine de diren�li olarak tespit edilmiştir. C.glabrata ve C.tropicalis izolatlarında flukonazol direnci g�r�lmezken, flukonazole en fazla azalmış duyarlılık (doza bağlı duyarlı ve diren�li) hem CLSI (24. saatte 8/67, %11.9; 48. saatte 12/67, %17.9) hem de EUCAST (19/67, %28.4) ile C.parapsilosis izolatlarında g�r�lm�şt�r. Anidulafungine azalmış duyarlılık (orta duyarlı ve diren�li) C.tropicalis izolatlarında %5.6, C.glabrata izolatlarında %3.3, C.albicans izolatlarında %2.7 olarak hem CLSI hem de EUCAST �nerileri ile uygulanan y�ntem ile saptanmıştır. C.parapsilosis izolatlarının ikisi EUCAST y�ntemi ile anidulofungine diren�li tespit edilmesine rağmen, CLSI y�ntemi ile duyarlı bulunmuştur (Tablo III).
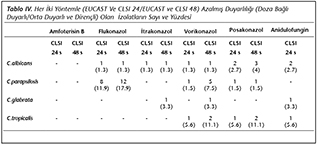
Tablo IV'te her iki y�ntemle azalmış duyarlılık (doza bağlı duyarlı/orta duyarlı ve diren�li) saptanan izolatların sayı ve y�zdeleri g�sterilmiştir. Buna g�re; amfoterisin B'ye iki y�ntemle de diren�li olarak saptanan herhangi bir izolat bulunmamıştır. Flukonazol diren�li C.albicans izolatının itrakonazol, posakonazol ve anidulafungine de diren�li olduğu g�r�lm�şt�r. Vorikonazole diren�li olan izolat ile anidulafungine diren�li olan diğer izolatın farklı olduğu g�zlenmiştir. Flukonazole diren�li C.parapsilosis izolatlarının; CLSI y�ntemine g�re 24. saat ink�basyonu ile bir tanesi (1/1), CLSI y�ntemine g�re 48. saat ink�basyonu ile �� tanesi (3/5) vorikonazole de diren�li bulunmuştur. CLSI y�ntemine g�re, 48. saatte vorikonazole diren�li diğer iki izolat ile posakonazole diren�li izolatın farklı olduğu saptanmıştır. CLSI y�ntemine g�re, 48. saatte C.glabrata izolatlarından birer tanesinde itrakonazol, vorikonazol ve anidulafungine diren� saptanmakla birlikte, bu izolatların aynı olmadığı tespit edilmiştir. C.tropicalis izolatlarında ise CLSI y�ntemine g�re hem 24. hem de 48. saatte saptanan vorikonazol ve posakonazole diren�li izolatların aynı olduğu g�zlenmiştir.
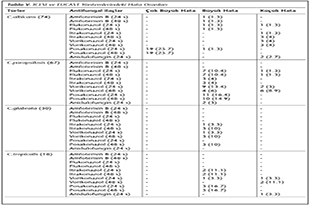
Tablo V'te CLSI ve EUCAST y�ntemleriyle �alışmamızda saptanan hata oranları g�sterilmiştir. �ok b�y�k hata, yalnız C.albicans izolatlarının posakonazol duyarlılığı i�in saptanmış, diğer ila�lar ve t�rlerde �ok b�y�k hata tespit edilmemiştir. B�y�k hataların �oğunluğu C.parapsilosis ve C.tropicalis izolatlarının azol grubu ila�larda g�zlenen sonu�larında g�r�lm�şt�r.
TARTIŞMA
Antifungal diren� gelişimini takip edebilmek i�in ulusal ve/veya uluslararası s�rveyans �alışmalarının yanı sıra b�lgesel merkezlerin antifungal duyarlılık durumunu bilmek ampirik tedaviye yol g�stermek a�ısından �nemlidir9. CLSI ve EUCAST rehberleri antifungal diren� gelişimini takipte kabul edilen iki referans y�ntemdir4,8. Bu �alışmada Uludağ �niversitesi Tıp Fak�ltesi Tıbbi Mikrobiyoloji Anabilim Dalı stoklarında bulunan Candida izolatlarının in vitro duyarlılığı CLSI ve EUCAST y�ntemleri kullanılarak değerlendirilmiştir.
Genel olarak her iki y�ntem arasındaki esas ve kategori uyumu 24. saatte daha iyi bulunmuştur ve bu durum CLSI y�nteminin son yıllarda yapılan 24. saat validasyonu ile uyumlu olarak g�zlenmiştir6. �zellikle, C.albicans ve C.tropicalis gibi hızlı �reyen t�rlerde 24 saatlik ink�basyonun yeterli olduğu ve �alışmamızda da C.albicans ve C.tropicalis izolatları a�ısından 24. saatte iki y�ntem arası uyum sorunu olmadığı saptanmıştır. Ancak, yavaş �reyen C.glabrata izolatları ve bazı C.parapsilosis izolatlarında iki y�ntem arasındaki uyum �zellikle flukonazol ve vorikonazol i�in 24. saatte d�ş�k bulunmuştur. Bu gibi durumlarda ink�basyonu 48. saate uzatmanın yararlı olabileceği d�ş�n�lm�şt�r. Uyumsuz izolatların �oğunlukla EUCAST y�ntemiyle saptanan MİK'leri daha y�ksek bulunmuştur. Bu olasılıkla iki y�ntem arasındaki farklılıktan �zellikle inok�lum farklılığından kaynaklanmaktadır10.
Kategori uyumunda en d�ş�k seviye C.albicans izolatlarının posakonazol duyarlılık sonu�larında g�zlenmiştir. Lipofilik �zelliği nedeniyle, bu ilacın ��z�n�rl�ğ�n�n d�ş�k olması ve bu nedenle iki y�ntemin karşılaştırılmasında zorluk oluştuğu başka �alışmalarda da bildirilmiştir. Benzer durum, itrakonazol duyarlılık sonu�ları i�in vurgulanmış olsa da, bu �alışmada itrakonazol kategorik uyumu a�ısından sorun tespit edilmemiştir11,12.
Flukonazol ve ekinokandinler kandidemi ve invaziv kandidozlarda ilk sırada tercih edilen ila�lardır13,14. Bu �alışmada kandidemi olgularından en sık izole edilen d�rt t�re ait izolatlarda anidulofungin direnci y�ksek bulunmamıştır. �zellikle Amerika Birleşik Devletleri ve Avrupa �lkelerinde %10'lara varan ve giderek artma eğiliminde olan C.glabrata izolatlarında g�r�len ekinokandin direnci bu �alışmada �nemli bir sorun olarak saptanmamıştır15,16. �lkemizde kan k�lt�rlerinden C.glabrata izolasyonu diğer �lkelere g�re daha azdır17-21. Bu a�ıdan izolasyonun d�ş�k olması ile direncin d�ş�k olmasının paralel olduğu d�ş�n�lebilir. Ancak, zaman i�inde izolasyonun ve direncin de artabileceği unutulmamalıdır. Merkezimizde farklı iki d�nemde yapılan kandidemi s�rveyans �alışmalarında her ne kadar C.glabrata izolasyon oranları d�ş�k olsa da yakın zamanı kapsayan ikinci �alışmada izolasyonda anlamlı artış olduğu saptanmıştır22,23.
C.glabrata t�rlerindeki flukonazol direnci �nemli bir diğer konudur. Bir�ok �alışmada y�ksek diren�ten bahsedilmesine rağmen, bu �alışmada C.parapsilosis hari� b�t�n diğer t�rlerde flukonazol direnci y�ksek seviyede bulunmamıştır24,25. Bu durum yine, C.glabrata'nın kan k�lt�rlerinden �ok fazla izole edilmemesi ile ilişkili olabilir. C.parapsilosis en fazla sağlık �alışanlarının ellerinde bulunmakta ve kateteri olan kritik hastalarda �nem taşımaktadır24. Flukonazol, C.parapsilosis t�rlerine iyi etki eden bir antifungaldir ve genellikle bu etkene karşı y�ksek diren� bildirilmemiştir. Bununla birlikte, Brezilya ve İspanya'da yapılan bazı �alışmalar, bizim �alışmamıza benzer şekilde C.parapsilosis izolatlarında saptanan flukonazol direncini bildirmiştir26,27. C.parapsilosis izolatlarının nozokomiyal enfeksiyona yol a�maları nedeniyle, diren�li izolatlar arasındaki klonal ilişkiyi saptamak epidemiyolojik a�ıdan �nemli olmaktadır.
Literat�rde, azol grubu ila�lar arasındaki �apraz diren�ten ve diğer b�t�n antifungallere de diren� gelişmesi ile oluşan panfungal diren�li izolatların saptandığı yayınlar bulunmaktadır28,29. Bu �alışmada da, C.parapsilosis izolatlarının bir kısmında �apraz olarak vorikonazole de diren� olduğu g�r�lm�şt�r. Bunun dışında bir C.albicans izolatında �oklu antifungal diren� (flukonazol, itrakonazol, posakonazol ve anidulafungin) saptanmıştır.
CLSI ve EUCAST y�ntemleri antifungal duyarlılıkta referans olarak kabul edilen iki y�ntemdir ve son yıllarda CLSI, klinik sınır değerleri d�ş�rerek ve 24 saatlik ink�basyonu valide ederek iki y�ntemin uyumunu arttırmaya �alışmıştır6. C.albicans, C.tropicalis, C.parapsilosis t�rlerinde flukonazol ile tamamen, vorikonazol ile kısmen [diren� sınırı iki y�ntemde faklıdır (CLSI ≥ 1 �g/ml; EUCAST ≥ 0.25 �g/ml)] bu uyumu sağlamıştır. Bu iki referans y�ntemin uluslararası �nemi nedeniyle uyumu artırma �abalarının diğer ila�lar ve t�rler i�in de devam etmesi �nemlidir30,31.
Tek merkezli olması, izolat sayısının nispeten azlığı ve diren�li izolatlarda diren� analizlerinin yapılamaması bu �alışmanın en �nemli eksiklikleridir. Ancak, kandidemilerde en sık izole edilen d�rt t�r ile �alışılmıştır ve lokal veri olarak hem hastanemize hem de �lkemize bu konuda katkı sağlayacağı d�ş�n�lmektedir.
Bu �alışmada, CLSI ve EUCAST rehberlerine g�re değerlendirilen antifungal duyarlılık sonu�larının 24 saatlik ink�basyon sonunda genellikle uyumlu olduğu, CLSI rehberine g�re uygulanan y�ntemle 24 saat ink�basyonla, C.parapsilosis ve C.glabrata gibi daha yavaş �reyen t�rlerde �zellikle vorikonazol ve flukonazol antifungalleri i�in bazen yeterli sonu� alınamadığı ve ink�basyonun uzatılması gerektiği, flukonazol ve ekinokandin direnci a�ısından sıkıntılı bir t�r olan C.glabrata'da şu an i�in �nemli bir sorun olmadığı, en �nemli sorunun C.parapsilosis izolatlarında tespit edilen flukonazol direncinin tespitinde yaşandığı belirlenmiştir.
Merkezler iki referans y�ntemden kendileri i�in uygun olanı se�erek antifungal duyarlılık �alışabilir. Ancak sonu�ları doğru okumak ve yorumlamak i�in �aba sarf edilmelidir. Diren�li bir izolat ile karşılaşıldığında farklı bir y�ntemle tekrar test edilerek direncin doğrulanması ve diren� mekanizmasının araştırılması konunun aydınlatılması a�ısından �nemlidir.
KAYNAKLAR
- Lass-Fl�rl C. The changing face of epidemiology of invasive fungal disease in Europe. Mycoses 2009; 52(3):197-205.
- Farina C, Manso E, Sanna S, et al. Management of antifungal susceptibility testing in Italy: comparative results of 2 nationwide surveys (1999 and 2004) in 102 Italian hospitals. Diagn Microbiol Infect Dis 2007; 57(2): 225-7.
- Johnson EM. Issues in antifungal susceptibility testing. J Antimicrob Chemother 2008; 61(Suppl 1): i13-8.
- Clinical and Laboratory Standards Institute (CLSI). Reference method for broth dilution antifungal susceptibility testing of yeasts: approved standard-third edition. CLSI document (M27-A3), 2008. CLSI, Wayne, PA.
- Clinical and Laboratory Standards Institute (CLSI). Reference method for broth dilution antifungal susceptibility testing of yeasts: 3rd informational supplement (M27-S3), 2008. CLSI, Wayne, PA.
- Pfaller MA, Diekema DJ. Progress in antifungal susceptibility testing of Candida spp. by use of Clinical and Laboratory Standards Institute broth microdilution methods, 2010 to 2012. J Clin Microbiol 2012; 50(9): 2846-56.
- Clinical and Laboratory Standards Institute (CLSI). Reference method for broth dilution antifungal susceptibility testing of yeasts: 4th informational supplement. 2012. CLSI, Wayne, PA.
- European Committee for Antimicrobial Susceptibility Testing (EUCAST). EUCAST definitive document E.Def 7.3: method for the determination of broth dilution MICs of antifungal agents for yeasts. 2015.
- Rodloff C, Koch D, Schaumann R. Epidemiology and antifungal resistance in invasive candidiasis. Eur J Med Res 2011; 16(4): 187-95.
- Cuenca-Estrella M, D�az-Guerra TM, Mellado E, Rodr�guez-Tudela JL. Influence of glucose supplementation and inoculum size on growth kinetics and antifungal susceptibility testing of Candida spp. J Clin Microbiol 2001; 39(2): 525-32.
- Espinel-Ingroff A, Pfaller M, Messer SA, Knapp CC, Holliday N, Killian SB. Multicenter comparison of the Sensititre YeastOne colorimetric antifungal panel with the NCCLS M27-A2 reference method for testing new antifungal agents against clinical isolates of Candida spp. J Clin Microbiol 2004; 42(2): 718-21.
- Pfaller MA, Espinel-Ingroff A, Jones RN. Clinical evaluation of the Sensititre YeastOne colorimetric antifungal plate for antifungal susceptibility testing of the new triazoles voriconazole, posaconazole, and ravuconazole. J Clin Microbiol 2004; 42(10): 4577-80.
- Pappas PG, Kauffman CA, Andes DR, et al. Executive Summary: Clinical practice guideline for the management of candidiasis: 2016 Update by the Infectious Diseases Society of America. Clin Infect Dis 2016; 62(4): 409-17.
- Ullmann AJ, Cornely OA, Donnelly JP, et al. ESCMID guideline for the diagnosis and management of Candida diseases 2012: developing European guidelines in clinical microbiology and infectious diseases. Clin Microbiol Infect 2012; 18(Suppl 7): 1-8.
- Pfaller MA, Castanheira M, Lockhart SR, Ahlquist AM, Messer SA, Jones RN. Frequency of decreased susceptibility and resistance to echinocandins among fluconazole-resistant bloodstream isolates of Candida glabrata. J Clin Microbiol 2012; 50(4): 1199-203.
- Alexander BD, Johnson MD, Pfeiffer CD, et al. Increasing echinocandin resistance in Candida glabrata: clinical failure correlates with presence of FKS mutations and elevated minimum inhibitory concentrations. Clin Infect Dis 2013; 56(12): 1724-32.
- Yapar N, Pulluk�u H, Oğuz VA, et al. Evaluation of species distribution and risk factors of candidemia: A multicenter case-control study. Med Mycol 2011; 49(1): 26-31.
- Aydın F, Bayramoğlu G, G�ler NC, Kaklıkaya N, Tosun İ. Bloodstream yeast infections in a university hospital in Northeast Turkey: a 4-year survey. Med Mycol 2011; 49(3): 316-9.
- Alp Ş, Arıkan-Akdağlı S, G�lmez D, Aşcıoğlu S, Uzun �, Akova M. Epidemiology of Candidaemia in a tertiary care university hospital: 10-year experience with 381 Candidaemia episodes between 2001 and 2010. Mycoses 2015; 58(8): 498-505.
- Horasan EŞ, Ers�z G, G�ksu M, et al. Increase in Candida parapsilosis fungemia in critical care units: a 6-years study. Mycopathologia 2010; 170(4): 263-8.
- Erdem İ, Oğuzoğlu N, �zt�rk Engin D, et al. Incidence, etiology and risk factors associated with mortality of nosocomial candidemia in a tertiary care hospital in Istanbul, Turkey. Med Princ Pract 2010; 19(6): 463-7.
- G�rc�oğlu E, Ener B, Akalın H, et al. Epidemiology of nosocomial Candidaemia in a university hospital: a 12-year study. Epidemiol Infect 2010; 138(9): 1328-35.
- Kazak E, Akın H, Ener B, et al. An investigation of Candida species isolated from blood cultures during 17 years in a university hospital. Mycoses 2014; 57(10): 623-9.
- Pfaller MA, Rhomberg PR, Messer SA, Jones RN, Castanheira M. Isavuconazole, micafungin, and 8 comparator antifungal agents' susceptibility profiles for common and uncommon opportunistic fungi collected in 2013: temporal analysis of antifungal drug resistance using CLSI species-specific clinical breakpoints and proposed epidemiological cutoff values. Diagn Microbiol Infect Dis 2015; 82 (4) : 303-13.
- Castanheira M, Messer SA, Rhomberg PR, Pfaller MA. Antifungal susceptibility patterns of a global collection of fungal isolates: results of the SENTRY Antifungal Surveillance Program (2013). Diagn Microbiol Infect Dis 2016; 85 (2): 200-4.
- da Costa VG, Quesada RMB, Abe ATS, Maria LF, Furlaneto MC. Nosocomial bloodstream Candida infections in a tertiary-care hospital in South Brazil: a 4-year survey. Mycopathologia 2014; 178(3-4): 243-50.
- Peman J, Canton E, Quindos G, et al. Epidemiology, species distribution and in vitro antifungal susceptibility of fungaemia in a Spanish multicentre prospective survey. J Antimicrob Chemother 2012; 67(5): 1181-7.
- Sanguinetti M, Posteraro B, Lass-Fl�rl C. Antifungal drug resistance among Candida species: mechanisms and clinical impact Mycoses 2015; 58 (Suppl. 2): 2-13.
- Pfaller M. Antifungal drug resistance: mechanisms, epidemiology, and consequences for treatment. Am J Med 2012; 125(1 Suppl): S3-13.
- Espinel-Ingroff A, Cuenca-Estrella M, Canton E. EUCAST and CLSI: working together towards a harmonized method for antifungal susceptibility testing. Curr Fungal Infect Rep 2013; 7(1): 59-67.
- Pfaller MA, Andes D, Diekema DJ, Espinel-Ingroff A, Sheehan D. Wild-type MIC distributions, epidemiological cutoff values and species- specific clinical breakpoints for fluconazole and Candida: time for harmonization of CLSI and EUCAST broth microdilution methods. Drug Resist Updat 2010; 13(6): 180-95.
İletişim (Correspondence):
Prof. Dr. Beyza Ener,
Uludağ �niversitesi Tıp Fak�ltesi
Tıbbi Mikrobiyoloji Anabilim Dalı,
G�r�kle, 16059 Bursa, T�rkiye.
Tel (Phone): +90 224 295 4113,
E-posta (E-mail): bener@uludag.edu.tr