Toxoplasmosis Ş�pheli Hastalara Ait Serolojik ve Molek�ler Test Sonu�larının
Retrospektif Olarak Değerlendirilmesi
Retrospective Evaluation of Serologic and Molecular Test Results of
Toxoplasmosis Suspected Patients
Emrah ERDOĞAN1, Merve Y�R�K1, Eda SİVCAN1, Serkan KARACA1, Hanife TEMEL1, Tuba ŞABANOĞLU1, Aslıhan G�LTEKİN1, İzzet ŞAHİN1
1 Erciyes �niversitesi Tıp Fak�ltesi, Tıbbi Parazitoloji Anabilim Dalı, Kayseri.
1 Erciyes University Faculty of Medicine, Department of Parasitology, Kayseri, Turkey.
Makale Atıfı: Erdoğan E, Y�r�k M, Sivcan E, Karaca S, Temel H, Şabanoğlu T ve ark. Toxoplasmosis Ş�pheli Hastalara Ait Serolojik ve Molek�ler Test Sonu�larının Retrospektif Olarak Değerlendirilmesi. Mikrobiyol Bul 2019;53(1):96-105
�Z
Hem sağlık hem de ekonomi a�ısından �nemli bir protozoon olan Toxoplasma gondii, �eşitli sıcakkanlı omurgalıları enfekte eden geniş bir konak yelpazesi olan zorunlu h�cre i�i parazittir. İnsanlar, kontamine su ve besinleri t�keterek, doku kisti i�eren �iğ veya az pişmiş etleri yiyerek, kan nakli, organ nakli ve transplasental ge�iş gibi değişik yollarla enfekte olabildiği i�in, toksoplazmozis son derece yaygın g�r�lmektedir. Bu �alışmada, toksoplazmozis ş�pheli hastalara ait serolojik ve molek�ler test sonu�larının retrospektif olarak değerlendirilmesi ama�lanmıştır. Erciyes �niversitesi Tıp Fak�ltesi, Tıbbi Parazitoloji Anabilim Dalı rutin seroloji ve molek�ler tanı laboratuvarlarımıza toksoplazmozis �n tanısı ile başvuran hastalardan alınan kan, beyin omurilik sıvısı (BOS), amniyon sıvısı, perikard sıvısı, apse �rneklerine anti-T.gondii-IgG ve anti-T.gondii-IgM ELISA, anti-T.gondii-IgM IFAT ve anti-T.gondii-IgG avidite serolojik testleri ve polimeraz zincir reaksiyonu (PCR) testleri uygulanmıştır. Taranan 6547 hastadan kadın hastaların %3.3'� (n= 220) yalnız IgM pozitifken, hem IgG hem de IgM pozitif olanların oranı %9.2 (n= 598) olarak tespit edilmiştir. Erkek hastalarda pozitiflik oranları daha d�ş�k olup yalnız IgM seropozitif hastalar %0.6 (n= 45) iken, hem IgG hem de IgM pozitif olan hastaların oranı %0.8 (n= 47) olarak belirlenmiştir. Toplam hasta sayısının %6.4'�n� (n= 425) oluşturan yenidoğanlarda IgG ve IgM antikorlarının pozitif olduğu olgu sayısı 20 (%0.3), tek başına IgM seropozitif olanların sayısı 25 (%0.4) olarak saptanmıştır. Yalnız IgM antikorları bakımından pozitif olan 290 hastaya ait �rneklerde Indirect Fluorescent Antibody Technique (IFAT) y�ntemi kullanıldığında bu hastaların 22'sinin anti-T.gondii-IFAT IgM pozitif olduğu tespit edilmiştir. Hastalarda IgM seropozitifliğine bakılmaksızın IgG antikorları bakımından pozitif olarak belirlenen hastalarda anti-T.gondii IgG avidite testi uygulanmış IgM negatif olan hasta serumlarının %0.7'sinde (n= 18) d�ş�k avidite, %6.5'inde (n= 179) sınırda avidite tespit edilmiştir. IgM pozitif hastaların %2.6'sında d�ş�k avidite tespit edilmiştir. Anti-T.gondii IgM negatif ve IgG pozitif olarak değerlendirilen olgulardan PCR ile dokuzu pozitif, ikisi negatif olarak saptanmıştır. Bu hastalardan birinin seroloji testi sonrası g�nderilen amniyon sıvısında PCR y�ntemiyle pozitif sonu� belirlenmiştir. PCR ile 20 BOS �rneğinde yedi �rnek pozitif olarak tespit edilmiştir. Ayrıca, anti-T.gondii IgM negatif ve IgG pozitif olduğu tespit edilen sekiz kan �rneğinin daha sonra yapılan PCR sonucuna g�re yedisinin pozitif ve birinin negatif olduğu tespit edilmiştir. Perikard sıvısı ve apse materyalleri ile �alışılan PCR testleri negatif olarak tespit edilmiştir. ELISA testlerinde oluşabilecek yanlış negatiflikler veya �apraz reaksiyon sonucu yanlış pozitiflikler gibi ş�pheli veya riskli durumlarda, altyapısı uygun olan laboratuvarların molek�ler temelli testleri uygulaması ile gereksiz ila� tedavisi veya girişimsel yaklaşımların �n�ne ge�ilebilir. Bu nedenle, riskli durumlarda serolojik testlere ek olarak molek�ler testlerin uygulanmasının daha g�venilir sonu�lar verebileceği kanısındayız.
Anahtar kelimeler: Toxoplasma gondii; ELISA; IFAT; avidite; PCR.
ABSTRACT
Toxoplasma gondii is a compulsory intracellular protozoan parasite with a wide range of host in warm-blooded vertebrates and has importance in terms of health and economy. Toxoplasmosis is very common because it can infect people with a variety of ways; ingestion of contaminated water and nutrients; raw or undercooked meats containing tissue cysts, blood transfusions, organ transplantantation and transplacental transfer. The aim of this study was to evaluate serologic and molecular test results of toxoplasmosis pre-diagnosed patients. Anti-T.gondii-IgG, anti-T.gondii-IgM ELISA, anti-T.gondii-IgM IFAT and anti-T.gondii-IgG avidity serological tests and PCR tests were applied by using blood, cerebrospinal fluid, amniotic fluid, pericardial fluid and abscess samples from patients who have admitted to Erciyes University Faculty of Medicine Department of Parasitology routine serology and molecular diagnosis laboratories with a pre-diagnosis of toxoplasmosis. Among 6547 patients 3.3% (n= 220) were only IgM positive, 9.2% were both IgG and IgM positive (n= 598). Among male patients, the positivity rates were lower and only IgM seropositive patients were 0.6% (n= 45) while the frequency of both IgG and IgM positive patients was 0.8% (n= 47). The number of both IgG and IgM seropositive cases among new borns, constituting 6.4% (n= 425) of the total number of patients, was 20 (0.3%) and the number of IgM seropositive samples was 25 (0.4%). Only 290 patients positive for IgM antibodies were studied for IFAT and 22 of these patients were positive for anti-T.gondii-IFAT IgM. Anti-T.gondii IgG avidity test was performed in all IgG positive patients regardless of their IgM seropositivity; low avidity was found in 0.7% (n= 18) of IgM-negative patients' sera and equivocal avidity was detected in 6.5% (n= 179). Low avidity was detected in 2.6% of IgM positive patients. Nine of the patients evaluated as anti-T.gondii IgM negative and IgG positive were detected as positive by PCR and two of them were negative. One of these PCR-positive patient's amniotic fluid was sent after the serological test results and detected as positive. Twenty CSF samples were studied by PCR and 7 samples were positive. Also, 8 blood samples which were anti-T.gondii IgM negative and IgG positive were found to bepositive in 7 and negative in one sample with PCR results, subsequently. PCR tests with pericardial fluid and abscess materials were found to be negative. In the case of suspicious or risky situations such as false negatives or false positives resulting from cross-reaction that can occur in ELISA tests, unnecessary medication or interventional approaches can be avoided by applying molecular-based testing at laboratories with appropriate infrastructure. For this reason, we believe that the application of molecular tests in addition to serological tests in risky situations may give more reliable results.
Keywords: Toxoplasma gondii; ELISA; IFA; avidity; PCR.
Geliş Tarihi (Received): 02.05.2018 - Kabul Ediliş Tarihi (Accepted): 13.11.2018
GİRİŞ
Toxoplasma gondii, �eşitli memeli ve kuş t�rlerini enfekte eden zorunlu h�cre i�i protozoon parazittir. T.gondii, geniş bir konak yelpazesi olan, sağlık ve ekonomi a�ısından �nem arz eden bir parazit olarak kabul edilmektedir. Hem kasaplık hayvanlarda hem de insanlarda transplasental olarak bulaşması sonucunda d�ş�k, �l� veya hastalıklı doğumlara neden olmaktadır. Ayrıca imm�nokompromize hastalarda diğer bir�ok organ tutulumu yanında beyin tutulumu sonucu oluşturduğu meningoensefalit tablosu ile �l�mlere sebep olmaktadır. İnsanlar enfeksiyonu, kontamine su ve besinleri t�keterek, doku kisti i�eren etleri �iğ veya az pişmiş şekilde yiyerek, kan nakli, organ nakli ve transplasental ge�iş gibi değişik yollarla alabildiği i�in, toksoplazmozis son derece yaygın g�r�lmektedir. Bu tip parazitozlarda toplumların gelenekleri ve beslenme alışkanlıkları hastalığın boyutlarını doğrudan etkileyen fakt�rler arasında �nemli bir yer tutmaktadır1-5.
�lkemizde yapılan �ok sayıda seroprevalans araştırması 40 yaşın �st�ndeki pop�lasyonda %60'ın �zerinde T.gondii seropozitifliği bulunduğunu g�stermektedir6. Sadece gebeler incelendiğinde, IgG pozitifliğinin %34-70 arasında değiştiği, d�ş�k, �l� doğum, erken doğum yapmış olanlarda ise %37-84 arasında bulunduğu bildirilmiştir6.
Toksoplazmozisin klinik belirtileri patognomonik olmayıp, yerleştiği organa g�re değişmektedir. Doğru tanı koyabilmek i�in değişik y�ntemler kullanılmaktadır. Bu y�ntemler, doğrudan ve dolaylı tanı y�ntemleri olmak �zere iki grup altında incelenebilir. Doğrudan tanı; etken izolasyonu, polimeraz zincir reaksiyonu (PCR), antijen spesifik lenfosit transformasyonu, lenfosit kopyalama tekniği ve histolojik y�ntemler ile yapılmaktadır. Dolaylı y�ntemler, T.gondii'ye �zg� antikorları belirlemek �zere kullanılan serolojik testleri kapsamaktadır. Olgunun durumuna g�re bu y�ntemlerden biri se�ilmektedir. V�cut sıvıları dışında diğer dokularda da PCR ile konjenital, ok�ler ve yaygın toksoplazmozisin tanısı konulabilmektedir. Konjenital toksoplazmozisde; gebenin toksoplazmozis tanısında, serolojik y�ntemler �ncelikli d�ş�n�lse de gebeliğin on sekizinci haftasından sonra amniyon sıvısında PCR �alışmak bebeğe bulaşın tanısında daha başarılı sonu� vermektedir. Amniyon sıvısında %65-80, plasenta �rneğinde %60, beyin omurilik sıvısı (BOS)'nda %17-100 ve ok�ler toksoplazmozis olgularında %100 oranında başarı sağlanmaktadır. Gebelik esnasında konjenital toksoplazmozis tanısı yalnız PCR ile konulabilmekte ve fare peritonu i�inde takizoitlerin �retimi ile PCR'nin beraber kullanımı %60 oranında başarı sağlamaktadır5. Hastalığın serolojik tanısı, enfeksiyonun genellikle subklinik seyrettiği durumlarda olduk�a �nem kazanmaktadır. Akut enfeksiyon sırasında ilk �nce IgM antikorları y�kselmektedir. Bu antikorlar 4 hafta i�inde en y�ksek seviyeye ulaştıktan sonra 6-8 aylık bir s�re�te gerilemektedir. IgG antikorları daha ge� oluşmaya başlayıp 1-2 ay i�inde en y�ksek seviyelerine ulaşmaktadır. N�ks olmayan durumlarda 2 yıl i�inde gerilemektedir. "Indirect Fluorescent Antibody Technique (IFAT)" y�ntemi canlı parazite ihtiya� duyulmaması nedeniyle avantajlıdır. IgM antikorlarını saptayarak akut toksoplazmozisi belirlemektedir. Dezavantajı pahalı gere�lere ihtiya� duyulmasıdır. ELISA, toksoplazmozisdeki fraksiyonları saptama olanağı ile akut-kronik toksoplazmozis ayrımı ve konjenital olguların takip edilmesinde tercih edilmektedir. G�n�m�zde toksoplazmozis tanısında ELISA'nın IgG, IgA ve IgE i�in �zelleşmiş alt t�rleri ve IgM i�in de "double sandwich" y�ntemi kullanılmaktadır. Konjenital toksoplazmozis ş�phesi ile doğan bebeklerde �eşitli radyolojik tetkiklerle konjenital toksoplazmozisin karakteristik belirtilerinden olan kafa i�i kalsifikasyon ve g�z tetkikleriyle koryoretinit taraması yapılmaktadır7-9.
�alışmada, toksoplazmozis ş�pheli hastalara ait serolojik ve molek�ler test sonu�larının retrospektif olarak değerlendirilmesi ama�lanmıştır.
GERE� ve Y�NTEM
Bu �alışma i�in Erciyes �niversitesi Klinik Araştırmalar Etik Kurulu Onayı (Tarih: 21.03.2018 ve Karar no: 208/168) alındı.
Hasta �rnekleri
Erciyes �niversitesi Tıp Fak�ltesi, Tıbbi Parazitoloji Anabilim Dalı rutin seroloji ve molek�ler tanı laboratuvarlarımıza toksoplazmozis �n tanısı ile başvuran hastalardan alınan kan, BOS, amniyon sıvısı, perikard sıvısı, apse �rneklerine serolojik ve molek�ler testler uygulandı. Buna g�re �alışmada, toksoplazmozis �n tanısı konulan 6547 hastanın verisi retrospektif olarak değerlendirildi.
Serolojik Testler
Anti-Toxoplasma gondii-IgG ve anti-T.gondii-IgM ELISA testleri i�in DIAPRO ticari kiti (Milano, İtalya) kullanıldı. T�m analiz işlemi imalat�ının �nerdiği şekilde ger�ekleştirildi. �rnekler, 1:100 oranında seyreltilerek ve kuyucuklara 100'er �l konuldu. Her kalibrat�r�n 100 �l'si ile negatif ve pozitif kontroller de kuyucuklara dağıtıldıktan sonra 37�C'de 1 saat ink�be edildi. Yıkamadan sonra, kuyucuklara 100 �l konjugat ilave edildi ve plaklar, 37�C'de 1 saat ink�be edildi. Son bir yıkama adımından sonra, antikorlar 100 �l "3,3',5,5'-Tetramethylbenzidine substrat ile tespit edildi. Reaksiyon 20 dakika sonra 100 �l 0.1 M H2O2 ile durduruldu ve plaklar bir ELISA okuyucuda 450 nm ile 620 nm dalga boyunda okundu. T�m serum �rnekleri analiz edildi. Anti-T.gondii-IgM IFAT i�in Euroimmune ticari kiti (L�beck, Almanya) kullanıldı. Serum �rnekleri, eurosorb ��zeltisinde vorteksleme ile y�zde 1:16 oranında seyreltildi ve daha sonra ticari kit işlemine g�re 3500 x g'da 5 dakika santrif�j edildi. Antijen kaplı preparatlara, 30 μl seyreltilmiş serum �rneklerinin supernatantı eklenerek 30 dakika oda sıcaklığında ink�be edildi. İnk�basyondan sonra preparatlar, 5 dakika boyunca PBS sol�syonu ile yıkandı ve 25 �l'lik konjuge antijen-antikorla kaplı alanlara eklendi. Karanlıkta oda sıcaklığında 30 dakika ink�be edildikten sonra yıkama işlemi tekrarlandı. Preparatlar 480 nm dalga boyundaki fl�oresan mikroskobu ile incelendi.
Anti-T.gondii-IgG avidite testi i�in Euroimmune (L�beck, Almanya) ticari kiti kullanıldı. Seyreltilmiş her serum �rneğinin 100 �l'si, negatif ve pozitif kontroller kuyucuklara �ift sıra halinde dağıtıldı ve oda sıcaklığında 30 dakika ink�be edildi. Sonra bir kez 300 �l yıkama ��zeltisi ile yıkandı, ardından �ift sıra halinde dağıtılmış olan �rneklerden ilk sıradaki kuyucuklara 200 �l fosfat, ikinci sıradaki kuyucuklara 200 �l �re eklendi. Oda sıcaklığında 10 dakika ink�be edildi. Sonra kuyucuklar tekrar 3 kez yıkandı. Kuyucuklara 100 �l konjuge eklenerek oda sıcaklığında 30 dakika ink�be edildi. Son yıkamadan sonra 100 �l TMB substrat eklendi. Tepkime, 15 dakika sonra 100 �l 0.1 M H2O2 ile durdurularak, kuyucuklar bir ELISA okuyucuda 450 nm ile 620 nm dalga boylarında okunarak, t�m serum �rnekleri analiz edildi.
Molek�ler Testler
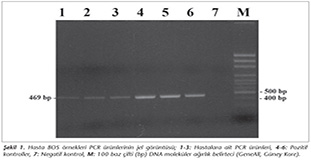
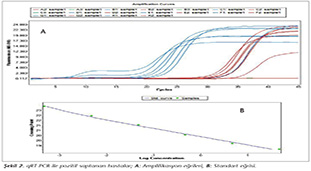
Hasta �rneklerinden 200 �l alınarak ticari kit (Qiagen, ABD) işlemine g�re DNA izolasyonu yapıldı. SYBR Green karışımı (2x) 10 �l, her bir primer 1 �l, kalıp DNA 5 �l, dH2O 3 �l olacak şekilde qPCR karışımı hazırlandı ve uygun sıcaklık d�ng�s�ne g�re ger�ekleştirildi (Tablo I). �rnekler aynı zamanda konvansiyonel PCR y�ntemi ile incelendi. Amplifikasyon tepkimeleri; 12.5 �l (2x) amplifikasyon karışımı, 5 �l kalıp DNA, her bir primer 1 �l olacak şekilde hazırlanan karışım ile ger�ekleştirildi (Tablo I). PCR �r�nleri %1.5 agaroz jelde y�r�t�ld� ve ardından DNA bantları g�r�nt�leme cihazında (Chemidoc MP, Biorad, ABD) g�r�nt�lendi ve değerlendirildi.
BULGULAR
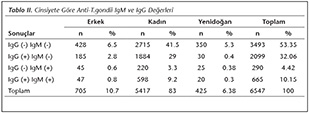
Bu �alışmada, 2013 Haziran-2017 Haziran tarihleri arasında farklı polikliniklerden gelen hasta �rneklerinin sonu�ları T.gondii pozitifliği y�n�nden taranmıştır. Serum �rneklerinde anti-T.gondii ELISA ile antikor aranmasının yanı sıra kan, BOS, amniyon sıvısı, perikard sıvısı, beyin apse materyallerinde PCR ve qPCR y�ntemleriyle T.gondii DNA varlığı araştırılmıştır. Taranan kadın hastaların %3.3'� (n= 220) yalnız IgM pozitifken, hem IgG hem de IgM pozitif olanların oranı %9.2 olarak bulunmuştur (n= 598). Erkek hastalarda pozitiflik oranları daha d�ş�k olup yalnız IgM seropozitif hastalar %0.6 (n= 45) iken, hem IgG hem de IgM pozitif olan hastaların oranı %0.8 (n= 47) olarak tespit edilmiştir. Toplam hasta sayısının %6.38'ini (n= 425) oluşturan yenidoğanlarda IgG ve IgM antikorlarının pozitif olduğu olgu sayısı 20 (%0.3), tek başına IgM seropozitif olanların sayısı 25 (%0.38) olarak belirlenmiştir (Tablo II).
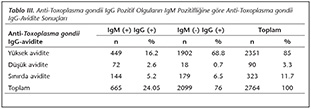
Hastalarda IgM seropozitifliğine bakılmaksızın IgG antikorları bakımından pozitif olarak belirlenen hastalarda anti-T.gondii IgG avidite testi �alışılarak IgM negatif olan hasta serumlarının %0.7'sinde (n= 18) d�ş�k avidite, %6.5'inde (n= 179) sınırda avidite tespit edilmiştir. IgM pozitif hastaların %2.6'sında d�ş�k avidite tespit edilmiştir. D�ş�k avidite akut enfeksiyon lehine olmakla beraber her zaman akut enfeksiyonu g�stermemektedir. Avidite mat�rasyonunda gecikmeler olabilmektedir. Bu nedenle, IgM pozitifliği olan 72 hastada daha muhtemel olmakla beraber, 90 hastanın olası akut toksoplazmozis bulgusu olan d�ş�k avidite değerlerine sahip olduğu saptanmıştır (Tablo III). Sadece IgM antikorları bakımından pozitif olan 290 hastaya IFAT �alışılmış ve bu hastaların 22'sinin anti-T.gondii-IFAT IgM pozitif olduğu tespit edilmiştir.
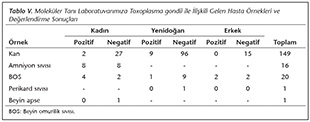
Farklı kliniklerden molek�ler y�ntemler ile inceleme yapılması i�in g�nderilen �rneklere (Tablo IV) doktor istemine bağlı olarak PCR ve qPCR y�ntemleri karşılaştırmalı uygulanmıştır. Buna g�re, 149 kan �rneği i�erisinden iki kadın hasta ve bir yenidoğan hasta �rneğinin sonucu pozitif olarak saptanmıştır (Şekil 1,Şekil 2). Molek�ler tanı laboratuvarımıza ulaştırılan toplam 16 farklı amniyon sıvısından sekizinin sonucu pozitif bulunmuştur. BOS materyalinin incelenmesi sonucunda d�rt kadın hasta, iki erkek hasta ve bir yenidoğan �rneği pozitif olarak değerlendirilmiştir. Kadın hastadan g�nderilen apse materyali ve yenidoğandan alınan perikard sıvısı negatif olarak belirlenmiştir (Tablo V). Anti-T.gondii IgM negatif ve IgG pozitif olarak değerlendirilen hasta gruplarına ait kan �rneklerinin dokuzu pozitifken, ikisi PCR ile negatif olarak saptanmıştır. Bu hastalardan birinin seroloji testi sonrası g�nderilen amniyon sıvısı ile PCR �alışılarak pozitif sonu� elde edilmiştir. Ayrıca, seronegatif sekiz �rneğin yedisi PCR ile pozitif olarak saptanırken, bir olgunun negatif sonu� verdiği tespit edilmiştir (Tablo VI). PCR pozitif olgulardan, serolojik testler sonucu yalnız IgG pozitifliği bulunan sekiz hastadan birinde sınırda avidite, geri kalanlarında y�ksek avidite, hem IgG hem de IgM pozitifliği bulunan bir hastada ise y�ksek avidite tespit edilmiştir.
TARTIŞMA
T.gondii, insan dahil memelileri ve kuşları enfekte edebilen, kozmopolit yayılışa sahip bir zoonozdur. Sıcak ve nemli yerlerde, soğuk ve kuru b�lgelere g�re daha y�ksek oranda g�r�lmektedir4. D�nyada bildirilen 38 salgın i�inde; su kaynaklı 8 (%21), toprakla temas kaynaklı 10 (%26.3), kontamine sebze t�ketimi kaynaklı 2 (%5.3), �iğ veya az pişmiş et t�ketimi kaynaklı 17 (%44.7) salgın bulunmaktadır. Avustralya, Brezilya, Kanada, Kore ve Amerika'da kistle kontamine �iğ veya az pişmiş et t�ketimine bağlı salgınlar; Kanada'da ve Brezilya'da ookistle kontamine su kaynaklı salgınlar; Brezilya'da, Amerika'da ve Birleşik Krallık'ta �iğ ke�i s�t� t�ketimine bağlı salgınlar bildirilmiştir10. Tayland'da ise gebe kadınlarda; yaş, i�me suyu kaynaklarının temizliği ve yerleşim yeri fakt�rlerinin seropozitifliğe etkili olduğu g�sterilmiştir11. T�rkiye'de gebelerde, doğurganlık �ağındaki kadınlarda, bazı y�relerde farklı yaş gruplarında ve değişik sosyoekonomik koşullara sahip bireylerde �ok sayıda seroprevalans araştırması yapılmıştır. Doğurganlık �ağındaki 943 olgunun retrospektif olarak değerlendirildiği �alışmada %28.5 anti-T.gondii IgG ve %0.9 anti-T.gondii IgM seropozitifliği belirlenirken, başka bir �alışmada 3 yıllık bir d�nemde toksoplazmozis ş�pheli gebe olan ve olmayan 1296 hastadan alınan kan �rneklerinde gebelerde %24.2 IgG ve %0.7 IgM, gebe olmayanlarda %37 IgG ve %0.9 IgM seropozitifliği saptanmıştır12,13. Benzer bir diğer �alışmada toplanan 322 �rneğin %63.4 IgG ve %4 IgM pozitifken gebelerde (n= 210) bu oranlar sırasıyla %39.5 ve %3.8 olarak tespit edilmiştir14. Gebelerde yapılan başka bir �alışmada yaş ortalaması 29 olan olguların IgG ve IgM pozitifliklerinin sırasıyla %28.8 ve %2.7 olduğu gebelerin %58.9'unun riskli davranış �yk�s� bulunduğu bildirilmiştir15. Diğer bir �alışmada ilk trimesterde 16-48 yaş aralığındaki 2011 gebe olguda TORCH taranması ile %31.4 IgG ve %0.8 IgM seropozitifliği bildirilmiştir6. Benzer bir başka �alışmada anti-Rubella ve anti-CMV pozitiflikleri saptanan gebelerde anti-T.gondii IgG ve IgM pozitiflikleri sırasıyla %43.9 ve %2.5 olarak tespit edilmiştir16. Anti-T.gondii antikorlarının araştırılması amacıyla başvuran 1-68 yaş aralığındaki 1887 olgunun %24'�nde pozitiflik saptanmış ve bu sonucun yaş artışı ile pozitif korelasyonu olduğu bildirilmiştir17. Başka bir �alışmada ise erkeklerde seropoziflik oranlarının kadınlara g�re nispeten daha d�ş�k olduğu g�sterilmiştir18. Tarımcılıkla uğraşan bir pop�lasyonda doğurganlık �ağındaki kadınlarda T.gondii seroprevalansının incelendiği bir �alışmada mevsimlik iş�i olarak tarım �alışanı olmanın, artan yaşın, �� veya daha fazla gebelik ge�irmiş olmanın, enfeksiyon riskini anlamlı oranda artırdığı g�sterilmiştir19.
Bu �alışmanın sonu�larının, literat�rdeki mevcut �alışmaların sonu�larını serolojik incelemeler bakımından destekler nitelikte olduğu tespit edilmiştir. Ancak, anti-T.gondii antikorları bakımından seronegatif g�r�len gebe ve yenidoğanlarda ELISA testinin doğrulanması i�in yapılan PCR testleri sonucunda sekiz olgunun yedisinin pozitif olduğu ve yalnız IgM seronegatif 11 olgunun yedisinin pozitif olduğu tespit edilmiştir. Bu, ELISA testinin molek�ler y�ntemler kadar duyarlı olmadığını g�stermektedir. Molek�ler testler ile pozitifliği saptanan hastaların serolojik test sonu�larına bakıldığında sekiz hastada yalnız IgG pozitifliği tespit edildiği ve bu olguların da sınırda veya y�ksek aviditesinin olduğu; hem IgG hem de IgM pozitifliği bulunan bir hastanın ise y�ksek aviditesi olduğu tespit edilmiştir. Rutin tanı laboratuvarında TORCH panelinde bulunan anti-T.gondii IgG ve IgM ELISA testleri, gebeliğin ilk trimesterinde olan hastalarda �alışılmaktadır. İki hafta sonra kan �rneklerinde yalnız IgM pozitifliği bulunan bu hastaların, tekrarlanan ELISA testi sonucunda bu durumun devam etmesi �zerine destekleyici bir test olarak kanda veya amniyon sıvısında qPCR testi �alışılmıştır. Anti-T.gondii IgM bakımından pozitif olduğu tespit edilen hastaların devam eden gebelik s�recinde bu testler ile takibi yapılmıştır. Bu durum, �oğunluğu gebelerden ve yenidoğanlardan oluşan olgularda rek�rens olabileceği ile a�ıklanabilir. Bununla birlikte, gebeliğinin ge� d�neminde serolojik test yapılan bir hastada, gebeliğin erken d�neminde ge�irilmiş bir enfeksiyona bağlı olarak oluşan IgM antikorları negatifleşmiş olabilir ancak bebekte intrauterin bulaş ger�ekleştiğinden �zellikle 18. haftadan sonra alınacak amniyon sıvısında �alışılan PCR ile doğru tanının konulabilmesi m�mk�n olabilir.
Sonu� olarak, ELISA test sonu�larının bu gibi durumlarda PCR ve qPCR sonu�ları ile karşılaştırılmalı olarak değerlendirilmesi gerektiği d�ş�n�lmektedir. ELISA testlerinde oluşabilecek yanlış negatiflik veya �apraz reaksiyon sonucu yanlış pozitiflik gibi ş�pheli veya riskli durumlarda, altyapısı uygun olan laboratuvarların molek�ler temelli testleri uygulaması ile gereksiz ila� tedavisinin veya girişimsel yaklaşımların �n�ne ge�ilebilir. Bu nedenle, riskli durumlarda serolojik testlere ek olarak molek�ler testlerin uygulanmasının daha g�venilir sonu�lar verebileceği kanısındayız.
�IKAR �ATIŞMASI
Yazarlar bu makale ile ilgili herhangi bir �ıkar �atışması bildirmemişlerdir.
KAYNAKLAR
- Kaye A. Toxoplasmosis: Diagnosis, treatment, and prevention in congenitally exposed infants. J Pediatr Health Care 2011;25(6):355-64.
- H�kelek M, A�ıcı, M. Toxoplasmosis, pp:803-30. In: Doğanay M, Altıntaş N (eds) Zoonozlar: Hayvanlardan insanlara bulaşan enfeksiyonlar. 2009, Vol:1. Bilimsel Tıp Yayınevi, Ankara.
- Saygı G. Paraziter hastalıklar ve parazitler, pp:143-54. 2009, Vol:1. Es Form Ofset Ltd. Şti, G�ztepe, İzmir.
- Doğan KB. Uzmanlık tezi: Gebelerde Toxoplasma gondii ve sitomegalovir�s seropozitiflik, serokonversiyon ve fetusa ge�iş oranının değerlendirilmesi. İn�n� �niversitesi Sağlık Bilimleri Enstit�s�, Malatya 2006.
- D�şkaya M, G�r�z Y. Toxoplasma gondii'de molek�ler yapı �alışmaları pp:429-52. In: �zcel M A, Tany�ksel M, Eren H (eds) Molek�ler Parazitoloji. 2009, Vol:1. Meta Basım Matbaacılık Hizmetleri, Bornova, İzmir.
- Doğan K, G�raslan H, �zel G, Aydan Z, Yaşar L. Gebelerde Toxoplasma gondii, Rubella, Sitomegalovir�s, Sifiliz ve Hepatit B seropozitiflik oranları. Turkiye Parazitol Derg 2014;38:228-33.
- Garcia LS. Diagnostic Medical Parasitology, pp:130-41. 2007, Vol:5. ASM Press, Washington.
- G�r�z Y, Delibaş SB. Toxoplasmosis ve İmm�nolojisi, pp:167-94. In: �zcel MA, Turgay N, İnci A, K�roğlu E (eds) Tıbbi ve veteriner imm�noparazitoloji. 2007, Vol:1. Meta Basım Matbaacılık Hizmetleri, Bornova, İzmir.
- Yazar S, Kuk S, Miman �, Saygı G. Saygı'nın temel tıbbi parazitoloji'si. 2016, 1. Baskı. Kayseri: Erciyes �niversitesi Yayınları.
- Meireles LR, Ekman CC, Andrade HF Jr, Luna EJ. Human Toxoplasmosis outbreak and the agent infecting form. Findings from a systematic review. Rev Inst Med Trop Sao Paulo 2015;57(5):369-76.
- Andiappan H, Nissapatorn V, Sawangjaroen N, Chemoh W, Lau YL, Kumar T, et al. Toxoplasma infection in pregnant women: a current status in Songklanagarind hospital, southern Thailand. Parasites Vectors 2014;7:239.
- Yazıcı V, Kale A, Malatyalı E, Ertabaklar H. Kocaeli Derince'de Toxoplasma gondii serolojisi i�in g�nderilen doğurganlık yaş grubundaki olgulara ait sonu�ların retrospektif olarak değerlendirilmesi. T�rkiye Parazitol Derg 2014;38:223-7.
- Selek MB, Bektore B, Baylan O, Ozyurt M. ���nc� basamak bir eğitim hastanesinde 2012-2014 yılları arasında gebelerde ve toksoplazmosis ş�pheli hastalarda Toxoplasma gondii'nin serolojik olarak araştırılması. T�rkiye Parazitol Derg 2015;39:200-4.
- Demiroğlu T, Polat ZA, Celik C. Kilis Devlet Hastanesi Kadın Doğum Polikliniğine başvuran doğurgan �ağdaki kadınlarda Toxoplasma gondii seropozitifliğine etki eden risk fakt�rlerinin araştırılması. T�rkiye Parazitol Derg 2015;39:299-304.
- Gencer M, Cevizci S, Sa�ar S, Vural A, Cakır G�ng�r AN, Uysal A, et al. �anakkale Onsekiz Mart �niversitesi Tıp Fak�ltesi Hastanesi Obstetri Polikliniğine m�racaat eden gebelerde anti-Toxoplasma gondii antikorlarının dağılımı ve risk fakt�rlerinin irdelenmesi. Turkiye Parazitol Derg 2014;38:76-80.
- Aynioglu A, Aynioglu O, Altunok ES. Seroprevalence of Toxoplasma gondii, Rubella and Cytomegalovirus among pregnant females in north-western Turkey. Acta Clinica Belgica 2015;70(5):321-4.
- Aşcı Z, Akg�n S. Afyon İlinde bir seroloji laboratuvarına Toxoplasma gondii (T.gondii) antikorları araştırılması amacıyla başvuran olgulara ait sonu�ların değerlendirilmesi. T�rkiye Parazitol Dergi 2015;39:9-12.
- Alver O, G�ral G, Ercan İ. Investigation of serological results of patients with suspected Toxoplasmosis admitted to the ELISA laboratory of Uludağ University Hospital between 2002-2008. Turkiye Parazitol Derg 2014;38:141-6.
- Doni NY, Simsek Z, Gurses G, Yıldız Zeyrek F, Demir C. Prevalence and associated risk factors of Toxoplasma gondii in female farm workers of southeastern Turkey. J Infect Dev Ctries 2015;9(1):87-93.
İletişim (Correspondence):
Dr. Emrah Erdoğan,
Erciyes �niversitesi Tıp Fak�ltesi,
Tıbbi Parazitoloji Anabilim Dalı,
Melikgazi 38039, Kayseri, T�rkiye.
Tel (Phone): +90 352 207 6666,
E-posta (E-mail): emrah@erciyes.edu.tr