Acinetobacter baumannii Kan İzolatlarının
MALDI-TOF MS, ARDRA ve blaOXA-51-benzeri
Gene Özgül Gerçek Zamanlı Polimeraz Zincir Reaksiyonu ile Tanımlanması
The Identification of Acinetobacter baumannii Blood Isolates
by MALDI-TOF MS, ARDRA and blaOXA-51-like Gene-Specific
Real-Time PCR
Ayşegül GÖZALAN1,Sibel AYDOĞAN2, Demet HACISEYİTOĞLU3, Çiğdem KUZUCU4, Fatma KÖKSAL5, Ziya Cibali AÇIKGÖZ6, Rıza DURMAZ6
1 Alanya Alaaddin Keykubat Üniversitesi, Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Antalya.
1Alanya Alaaddin Keykubat University Faculty of Medicine, Department of Medical Microbiology, Antalya, Turkey.
2Ankara Şehir Hastanesi, Tıbbi Mikrobiyoloji Laboratuvarı, Ankara.
2Ministry of Health Ankara City Hospital, Laboratory of Medical Microbiology, Ankara, Turkey.
3Bülent Ecevit Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Zonguldak.
3Bulent Ecevit University Faculty of Medicine, Department of Medical Microbiology, Zonguldak, Turkey.
4İzmir Tınaztepe Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, İzmir.
4İzmir Tınaztepe University Faculty of Medicine, Department of Medical Microbiology, İzmir, Turkey.
5İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, İstanbul.
5Istanbul University Cerrahpaşa Faculty of Medicine, Department of Medical Microbiology, İstanbul, Turkey.
6Yıldırım Beyazıt Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Ankara, Türkiye.
6Yıldırım Beyazıt University Faculty of Medicine, Department of Medical Microbiology Ankara, Turkey.
*Bu çalışma, 5. Ulusal Klinik Mikrobiyoloji Uzmanlık Derneği (KLİMUD) Kongresi (28 Ekim-1 Kasım 2019, İzmir)’nde sözlü olarak sunulmuştur. Bu çalışma, Türkiye Bilimsel ve Teknolojik Araştırma Kurumu (TÜBİTAK) 3001 Başlangıç Ar-Ge 116S249 proje numarası ile desteklenmiştir.
Makale Atıfı: Gözalan A, Aydoğan S, Hacıseyitoğlu D, Kuzucu Ç, Köksal F, Açıkgöz ZC ve ark. Acinetobacter baumannii kan izolatlarının MALDI-TOF MS, ARDRA ve blaOXA-51-benzeri gene özgül gerçek zamanlı polimeraz zincir reaksiyonu ile tanımlanması. Mikrobiyol Bul 2020;54(4):535-546.
ÖZ
Acinetobacter calcoaceticus-Acinetobacter baumannii (Acb) kompleks; fenotipik olarak ayırt edilemez düzeyde benzer kabul edilen hastane kaynaklı enfeksiyon etkenleri olan A.baumannii, Acinetobacter nosocomialis, Acinetobacter pittii, Acinetobacter seifertii ve Acinetobacter djikshoorniae türleri ile çevresel bir tür olan A.calcoaceticus’tan oluşmaktadır. Acb kompleks içerisindeki türlerin antimikrobiyal duyarlılık ve klinik sonuçları farklı olduğu için tür düzeyinde tam ve doğru tanımlanmaları önemlidir. Konvansiyonel fenotipik yöntemler, en önemli klinik tür olan A.baumannii de dahil olmak üzere Acb kompleks üyesi türlerin tanımlanması için zaman alıcı, güvenilirlik ve yeterliliği düşük yöntemlerdir. Acb kompleks türlerinin tanımlanması için çoğaltılmış ribozomal DNA kesim analizi [amplified ribosomal DNA restriction analysis (ARDRA)] ve blaOXA-51-benzeri genine özgül polimeraz zincir reaksiyonu (PCR) gibi güvenilir moleküler yöntemlerin rutin tanı laboratuvarlarında kullanımı çoğu zaman mümkün olmamaktadır. Son yıllarda, klinik laboratuvarlarda bakteri türlerinin tanımlanması için hızlı, düşük maliyetli ve kullanışlı matriks ile desteklenmiş lazer dezorpsiyon iyonizasyon uçuş zamanı kütle spektrometresi [matrix-assisted laser desorption ionization-time of flight mass spectrometry (MALDI-TOF MS)] yöntemi geliştirilmiştir. Bu çalışmada, A.baumannii kan izolatlarının tanısında MALDI-TOF yönteminin tanı performansını değerlendirmek amaçlanmıştır. Çalışmaya, Ocak 2016-Aralık 2016 tarihleri arasında, üniversite hastanelerinin yoğun bakım ünitelerinden izole edilen 180 adet tekrarlamayan karbapenem dirençli Acb kompleks (izolat numaraları: TR1-TR60) ve A.baumannii (TR61-TR180) kan izolatı alınmıştır. Tüm izolatlar, blaOXA-51-benzerigene özgül gerçek zamanlı PCR (Rt-PCR), ARDRA (kesim enzimleri-AluI, CfoI, MboI MspI, RsaI) ve MALDI-TOF MS (VITEK® MS, bioMérieux, Fransa) yöntemleri ile değerlendirilmiştir. ARDRA yöntemiyle TR10, TR31, TR35 ve TR52 izolatları dışında tüm izolatlar A.baumannii olarak tanımlanmıştır. Tüm izolatlardan TR10, TR31 ve TR52 dışında kalan 177 izolatta blaOXA-51-benzeri gen varlığı saptanmıştır. blaOXA-51-benzeri gen varlığı gösterilemeyen bir izolat (TR31), ARDRA yöntemi ile A.pittii olarak tanımlanmıştır. ARDRA ve blaOXA-51-benzeri gene özgül Rt-PCR yöntemlerinin birlikte A.baumannii olarak tanımladığı 176 izolat referans kabul edilerek, MALDI-TOF yönteminin tanı kapasitesi değerlendirilmiştir. Toplam 176 izolat için MALDI-TOF yönteminin duyarlılığı %99.4, özgüllüğü ise %75 olarak bulunmuştur. Yöntemin, A.baumannii’nin tür düzeyinde tanımlanması için doğruluk değeri %98.9 olarak hesaplanmıştır. MALDI-TOF sistemi, rutin tanı laboratuvarlarında giderek artan oranlarda kullanılan, bakterilerin cins, tür ve alt tür düzeyinde tanımlanmalarına olanak sağlayan yüksek duyarlılık ve özgüllüğe sahip bir yöntemdir. MALDI-TOF yönteminin, veri tabanlarının geliştirilmesiyle, gelecekte rutin tanı laboratuvarlarında daha fazla türü tanımlayabilen, bakterilerde antibiyotik direnç ve virülans belirteçlerini test edebilen ideal bir sistem olacağını düşünüyoruz.
Anahtar kelimeler: Acinetobacter baumannii; polimeraz zincir reaksiyonu; çoğaltılmış ribozomal DNA kesim analizi; matriks ile desteklenmiş lazer dezorpsiyon iyonizasyon; kütle spektrofotometresi.
ABSTRACT
The Acinetobacter calcoaceticus-Acinetobacter baumannii (Acb) complex consists of phenotypically very similar nosocomial species; A.baumannii, Acinetobacter nosocomialis, Acinetobacter pittii, Acinetobacter seifertii and Acinetobacter djikshoorniae and one environmental species A.calcoaceticus. The rapid and accurate identification of the members of Acb complex is critical as these nosocomial pathogens can show differences in antimicrobial susceptibility and clinical outcomes. The conventional phenotypic methods are slow, unreliable and less efficient for the differentiation of Acb complex species, including the A.baumannii species within the Acb complex. Although various molecular methods are available, such as amplified ribosomal DNA restriction analysis (ARDRA) and blaOXA-51-like gene specific PCR, they are usually inconvenient for the routine diagnostic laboratories. Recently, matrix-assisted laser desorption ionization-time of flight mass spectrometry (MALDI-TOF MS) offers an opportunity for rapid, cost-effective and convenient bacterial identification in routine diagnostic procedures conducted in clinical laboratory. In this study, we aimed to evaluate the diagnosis performance of MALDI-TOF MS system to identify blood isolates of A.baumannii. A total of 180 non-duplicate carbapenem resistant Acb complex (strain numbers; TR1-TR60) and A.baumannii (TR61-TR180) blood isolates were collected from the intensive care units of the three university hospitals in Turkey from January 2016 to December 2016. All isolates were evaluated by using blaOXA-51-like gene specific real time (Rt-PCR) analysis, ARDRA (restriction enzymes-AluI, CfoI, MboI, MspI, RsaI) method and MALDI-TOF MS (VITEK® MS, bioMérieux, France) system. All the strains except TR10, TR31, TR35 and TR52 were identified as A.baumannii by ARDRA method. Out of 177 of all the isolates, presence of blaOXA-51-like gene was found except for TR10, TR31 and TR52 isolates. However, TR31 without the presence of blaOXA-51-like gene was identified as A.pittii using the ARDRA. Totally 176 isolates which were identified as A.baumannii by both of the methods, ARDRA and Rt-PCR- blaOXA-51-like, were accepted as a reference for the evaluation of the diagnosis performance capacity of the MALDI-TOF MS. Overall, for all 176 isolates tested, the sensitivity obtained with the MALDI-TOF MS were 99.4% with 75% specificity. The accuracy value of the method was determined as 98.9% for the identification of A.baumannii to the species level. MALDI-TOF MS is increasingly used in diagnostic microbiology for the routine identification of bacteria to the genus, species or subspecies level with high rates of sensitivity and specificity. In future, by expanding the database, MALDI-TOF MS system would possibly become the ideal method for routine diagnostic laboratories that could potentially identify more species and even determine some characteristics of antimicrobial resistance and virulence determinants.
Keywords: Acinetobacter baumannii; polymerase chain reaction; amplified ribosomal DNA restriction analysis; matrix-assisted laser desorption-ionization; mass spectrometry
Geliş Tarihi (Received): 02.07.2020 - Kabul Ediliş Tarihi (Accepted):30.09.2020
GİRİŞ
Acinetobacter cinsi bakteriler gram-negatif, nonfermentatif ve zorunlu aerop mikroorganizmalardır. Günümüzde halen Acinetobacter cinsi içerisinde 63 farklı tür bulunmaktadır[1]. Acinetobacter cinsi içerisinde hastane kaynaklı enfeksiyonlardan sorumlu türler arasında Acinetobacter baumannii, Acinetobacter nosocomialis, Acinetobacter pittii ve çevresel bir tür olan Acinetobacter calcoaceticus bulunmaktadır. Bu türler, fenotipik ve biyokimyasal olarak ayırt edilemez düzeyde benzer özelliklere sahiptir. Genotipik olarak farklılık gösteren ancak fenotipik olarak ayırt edilemez olan bu türler, A.calcoaceticus-A.baumannii kompleks (Acb kompleks) olarak adlandırılmıştır[2].
Son yıllarda, Acb kompleks içerisine iki yeni patojenik tür; A.baumannii ve A.nosocomialis ile yakın ilişkili Acinetobacter seifertii ve A.pittii ile yakın ilişkili olan Acinetobacter dijkshoorniae dahil edilmiştir[3],[4]. Acb kompleks içerisindeki türlerin kolonizasyon ve patojenite yetenekleri ile antimikrobiyal duyarlılık ve klinik sonuçları farklı olduğu için bunların tam ve doğru tanımlanmaları önemlidir. Acinetobacter cinsi içerisinde antibiyotik direnci ve mortalitesi en yüksek tür A.baumannii’dir. A.baumannii’nin son yıllarda kolistin, polimiksin B ve tigesiklin dahil hemen tüm antibiyotiklere direnç geliştirdiği bildirilmektedir[5].
Acinetobacter türlerinin tanımlanması için biyokimyasal yöntemler ve otomatize sistemlerin güvenilirliği düşüktür. Günümüzde, Acb kompleks içerisindeki türlerin tanımlanması için kullanılan moleküler yöntemler; çoğaltılmış ribozomal DNA kesim analizi [amplified ribosomal DNA restriction analysis (ARDRA)][6],[7] “16S-23S rRNA intergenic spacer (ITS)” ve recA dizi analizi[8],[9],, DNA giraz B gen (gyrB) dizi analizi[10] ve RNA polimeraz ß-subunit gen (rpoB) dizi analizidir[11]. A.baumannii’nin tanımlanmasında basit ve güvenilir moleküler yöntemlerden biri de bu mikroorganizmaya özgül intrinsik blaOXA-51-benzeri genlerinin polimeraz zincir reaksiyonu (PCR) ile gösterilmesidir[12],[13].
Acinetobacter türlerinin tanımlanması için moleküler yöntemlerin rutin tanı laboratuvarlarında kullanımı her zaman mümkün olamamaktadır. Son yıllarda, klinik laboratuvarlarda bakteri türlerinin tanımlanması için ribozomal proteinleri temel alan matriks ile desteklenmiş lazer dezorpsiyon iyonizasyon uçuş zamanı kütle spektrometresi [matrix-assisted laser desorption ionization-time of flight mass spectrometry (MALDI-TOF MS)] yöntemi geliştirilmiştir. MALDI-TOF MS sisteminin, rutin klinik laboratuvarlarında bakteriyel tanımlama için hızlı, uygun maliyetli, kullanışlı ve yüksek verimlilikte olduğu bildirilmektedir[13],[14].
Bu çalışmada, üç farklı bölgede bulunan üniversite hastanelerinin yoğun bakım ünitesi (YBÜ) hastalarından izole edilen A.baumannii kan izolatlarının tanısında MALDI-TOF MS temelli VITEK® MS (bioMérieux, Marcy l’Etoile, Fransa) ve referans moleküler yöntemlerin karşılaştırılması amaçlanmıştır.
GEREÇ ve YÖNTEM
Bu çalışma, Yıldırım Beyazıt Üniversitesi Klinik Araştırmalar Etik Kurulu onayı ile gerçekleştirildi (Tarih: 17.02.2016 ve Karar no: 33).
Bu çalışma, Ankara, Malatya ve İstanbul Tıp Fakültesi hastanelerinde gerçekleştirilen çok merkezli bir çalışma olarak planlandı. Ocak 2016-Aralık 2016 tarihleri arasında YBÜ’lerde tedavi gören hastaların kan örneklerinden izole edilen karbapenem dirençli Acb kompleks (izolat numaraları: TR1-TR60) ve A.baumannii (TR61-TR180) izolatları araştırmaya dahil edildi. Her hastanın yalnız tek bir örneğinden elde edilen izolatlar o merkeze ait -20°C derin dondurucularda saklandı (Tablo 1).
DNA İzolasyonu
A.baumannii izolatları %5 koyun kanlı agara ekildi, plaklar 37°C’lik etüvde 16-18 saat üremeye bırakıldı. Üreyen bakteriler eküvyon ile toplanıp 500 µl fosfat tamponu (PBS) içeren mikrosantrifüj tüplerine aktarıldı. Sonrasında vortekslenen tüpler, DNA izolasyonu için ısı bloğunda 100°C’de 10 dakika tutuldu. Ardından 10.000 rpm’de 1 dakika çevrilerek süpernatan DNA olarak kullanıldı. DNA örnekleri, kullanılıncaya kadar -80°C’lik derin dondurucuda saklandı.
ARDRA Yöntemi ile Tanımlama
PCR reaksiyon karışımı toplam 50 µl hacimde hazırlanarak, içerisine 25 µl 2X PCR master mix-DreamTaq Green PCR (ThermoFisher Scientifics, Life Technologies, ABD) ve her bir primerden 10 pmol ve 5 µl kalıp DNA konuldu. Çalışmada kullanılan primerler 16S rDNA bölgesine yönelik olup, dizileri 5’-TGG CTC AGA TTG AAC GCT GGC GGC-3’forward ve 5’-TAC CTT GTT ACG ACT TCA CCC CA-3’reverse şeklindedir[6]. PCR, CFX96 (Bio-Rad, Herculs, ABD) gerçek zamanlı PCR (RT-PCR) cihazında gerçekleştirildi. PCR döngüleri; 95˚C’de 3 dakika ilk denatürasyonu takiben, 40 döngü 30 saniye 95˚C’de denatürasyon, 30 saniye 60˚C’de bağlanma, 1 dakika 72°C’de amplifikasyon işlemleri ve son olarak da 72°C’de 10 dakika uzama şeklinde uygulandı.
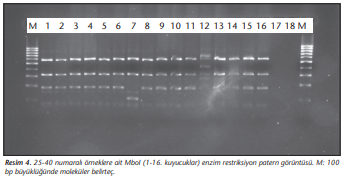
Amplifikasyon ürünleri %2’lik agaroz 3:1 jelde 30 dakika yürütüldükten sonra Molecular Imager® GelDoc TM XR+ (BioRad, ABD) görüntüleme sistemi ile değerlendirildi. Yaklaşık 1.500 baz çifti (bp) büyüklüğünde bantların varlığı pozitif olarak değerlendirildi. Her çalışmada, negatif kontrol olarak steril ultra saf su ve pozitif kontrol olarak A.baumannii ATCC19606 suşu kullanıldı.
Amplifikasyon ürününden 9 µl, 5 U restriksiyon enzimi içeren 20 µl restriksiyon tamponu (Promega, ABD) içerisinde 37°C’de dört saat inkübe edilmiştir. Restriksiyonu sonlandırmak için 5 ml 5X sample buffer [gliserol, %25 (wt/vol), sodyum dodesil sülfat, %0.5 (wt/vol), EDTA, 50 mM; bromfenol blue, %0.05] eklendi. Restriksiyon fragmanları %2.5’lik Nusieve agaroz 3:1 jel kullanılarak görüntülenmiş ve elde edilen sonuçlar değerlendirilmiştir[6],[7]. Çalışmada A.baumannii ATCC 19606 suşu pozitif kontrol olarak kullanılmıştır. Enzim kesimi için AluI, CfoI, MboI MspI, RsaI enzimleri kullanılmıştır. Ön çalışma için beş örnekte (156, 163-166) enzimlerin hepsiyle kesim yapıldıktan sonra sonuçlar literatür bilgisi eşliğinde değerlendirildi, MspI ve RsaI enzimlerinin ARDRA profilini belirlemede ek bir bilgi sağlamadığı anlaşılarak, kalan örnekler için AluI, CfoI, MboI enzimleri ile çalışmaya devam edildi[6].
blaOXA-51-benzeri Genine Özgül Gerçek Zamanlı Polimeraz Zincir Reaksiyonu Analizi
PCR reaksiyon karışımı toplam 25 µl hacimde, içerisinde 12.5 µl 2XPCR karışımı (Thermo Scientific Maxima SYBR GReen/ROX pPCR Master Mix, Life Technologies, ABD), her biri 12.5 pmol olan primer ve 5 µl kalıp DNA konuldu. PCR sırasında kullanılacak olan blaOXA-51-benzeri gen bölgesine yönelik primer dizileri; blaOXA-51-benzeri F için 5’-TAA TGC TTT GAT CGG CCT TG-3’ ve blaOXA-51-benzeri R için 5’-TGG ATT GCA CTT CAT CTT GG-3’ şeklinde kullanıldı[15].
PCR döngüleri; 95˚C’de 10 dakika ilk denatürasyonu takiben, 40 döngü 15 saniye 95˚C’de denatürasyon, 30 saniye 60˚C’de primer bağlanması, 1 dakika 72°C’de amplifikasyon ve ardından 72˚C’de 5 dakika uzama şeklinde uygulandı.
SYBR Green içeren Rt-PCR’nin kullanıldığı aşamada amplifikasyon, Rotor Gene 6000 platform (Corbett Research, Avustralya) Rt-PCR cihazında gerçekleştirildi. Bağlanma ve uzama aşamalarında sinyal toplama programı uygulandı. Çalışmada, A.baumanniiAcinetobacter baumannii ATCC 19606 suşu pozitif kontrol olarak kullanıldı[12],[16].
MALDI-TOF MS Sistemi ile Tanımlama
Derin dondurucudan çıkarılan izolatlar, %5 koyun kanlı besiyerine iki kez pasajlanarak 35°C’de ve aerobik ortamda inkübe edildi. Üreyen bu kolonilerden alınan bir parça, MALDI-TOF sisteminin (VITEK® MS, bioMérieux, Fransa) slaytlarındaki kuyucuklara ince bir tabaka şeklinde yayıldı ve üzerine 1 μL matriks solüsyonu (𝛼’-Cyano-4-hydroxy-cinnamic acid= C.H.C.A.) (bioMérieux, Fransa) damlatıldı. Her bir koloniden iki adet yayma hazırlandı. Yaymalardan biri tanımlama için kullanılırken, diğeri gereksinim olduğunda kullanılmak üzere hazır tutuldu. Firmanın kullanım önerisi doğrultusunda, her 16 kuyucuk için 1 adet Escherichia coli ATCC 8739 suşu kullanıldı. Bu slaytlar daha sonra MALDI-TOF sistemine (VITEK® MS, bioMérieux, Fransa) bakterinin tanımlanması için yüklendi. Slaytlara yayılan bakteriler, süre sonunda bu sistemin kullandığı MYLA® software v3.2. (bioMérieux, Fransa) yardımıyla kütüphanesindeki bakterilerle kıyaslanması yoluyla değerlendirilerek isimlendirildi. Uyum oranı %90’ın üzerinde olan izolatların tanımlanmaları kabul edildi.
İstatistiksel Analiz
Verilerin analizinde SPSS versiyon 23.0 (IBM, Armonk, ABD) yazılımı kullanıldı. ARDRA ve Rt-PCR-blaOXA-51-benzeri yöntemlerinin birlikte A.baumannii olarak tanımladığı izolatlar referans kabul edilerek, MALDI-TOF MS yönteminin performans kapasitesi [geçerlilik; duyarlılık, özgüllük, pozitif prediktif değer (PPD) ve negatif prediktif değer (NPD)] hesaplandı.
BULGULAR
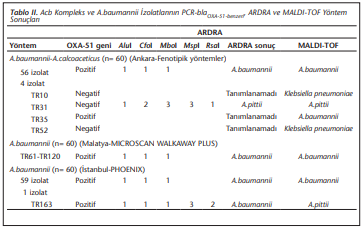
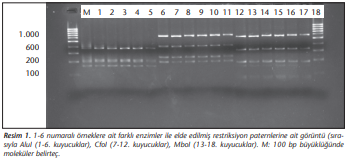
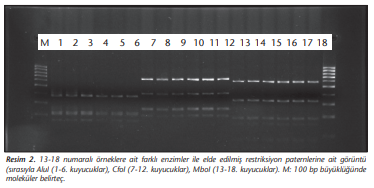
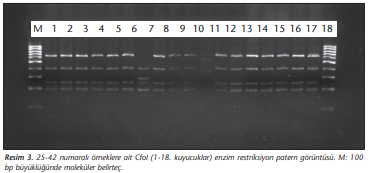
ARDRA yöntemiyle 180 izolattan dördü (TR10, TR31, TR35 ve TR52) dışında tüm izolatlar A.baumanniiAcinetobacter baumannii olarak tanımlanmıştır. TR31 izolatı dışında, tüm izolatlarda sırasıyla; AluI, CfoI, MboI enzimleri için 1,1,1 paternleri saptanmıştır. Otuz bir numaralı örnek için ise AluI, CfoI, MboI, Mspl ve Rsal enzimleri için sırasıyla 1, 2, 3, 3, 1 paternleri elde edilmiş ve A.pittii olarak tanımlanmıştır (Tablo 2). ARDRA 16S rRNA gen kesim paternlerine ait görüntüler sırasıyla (Resim 1)-(Resim 4)’te verilmiştir.
Çalışmaya alınan izolatlardan 177’sinde blaOXA-51-benzeri geni saptanmıştır. Üç izolatta blaOXA-51-benzeri geni saptanamamıştır. Bu izolatlardan ikisi (TR10 ve TR52) MALDI-TOF MS ile Klebsiella pneumoniae olarak tanımlanmıştır. blaOXA-51-benzeri geni saptanamayan üçüncü izolat (TR31), ARDRA ve MALDI-TOF MS ile A.pitti olarak tanımlanmıştır. ARDRA ile tanımlanamayan izolatta (TR35); blaOXA-51-benzeri geni saptanmış ve MALDI-TOF MS ile A.baumannii olarak belirlenmiştir (Tablo 2).
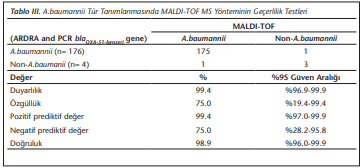
ARDRA ve Rt-PCR-blaOXA-51-benzeri yöntemlerinin birlikte A.baumanniiolarak tanımlandığı izolatlar referans kabul edilerek MALDI-TOF MS yönteminin tanı performans kapasitesi değerlendirilmiştir. VITEK® MS yöntemi ileA.baumannii türlerinin %99.4’ünün doğru tanımlandığı saptanmıştır (Tablo 3).
TARTIŞMA
Acinetobacter calcoaceticus-Acinetobacter baumannii kompleks (Acb kompleks); A.calcoaceticus (genomic species 1), A.baumannii (genomic species 2), A.pittii (genomic species 3) ve Acinetobacter nosocomialis (genomic species 13TU) türlerini içermektedir[17]. Acb kompleksinde yer alan türlerin epidemiyolojik özellikleri, antibiyotik duyarlılık profilleri ve klinikteki uyumları farklılıklar göstermektedir. Dolayısıyla hastane kaynaklı enfeksiyonlara yol açan bu türlerin tanımlanması, tedavi yaklaşımları ve enfeksiyon kontrol önlemlerine yön vermesi açısından önemlidir[18] .
Acb kompleks içerisindeki en önemli klinik tür olan A.baumannii’nin tanımlanması için rutin laboratuvarlarda kullanılan standart biyokimyasal testler ve otomatize sistemler düşük güvenirliliği olan yöntemler olarak kabul edilmektedir. Moleküler yöntemler ise Acinetobacter türlerinin ayrımında güvenilir fakat yalnızca referans laboratuvarlarda uygulanabilen ve maliyetli tekniklerdir[19].
Acinetobacter türlerinin ayrımında ”güvenilir belirleyici” olarak kabul edilen intrinsik karbapenem direnç geni blaOXA-51 ilk olarak 2005 yılında Brown ve arkadaşları[20] tarafından tanımlanmıştır. Daha sonra, bu genin pek çok varyantı olduğu gösterilmiş ve tüm varyantları blaOXA-51-benzeri başlığı altında toplanmıştır[12].
A.baumannii’nin tür düzeyinde tanımlanmasında intrinsik blaOXA-51-benzeri gen varlığının bir biyobelirteç olarak kullanılabileceği ilk olarak Turton ve arkadaşları[12] tarafından bildirilmiştir. Çalışmaya alınan 106 A.baumannii klinik izolatı ve ATCC 19606 suşunda PCR yöntemi ile blaOXA-51-benzeri geni varlığı tespit edilirken, diğer türlerde bu genin bulunmadığı saptanmıştır[12].
Bununla birlikte, PCR yönteminin, blaOXA-51-benzeri geninin bugüne kadar tanımlanan tüm varyantlarını tespit edememe gibi bir sınırlaması olduğu bilinmektedir[12],[21]. blaOXA-51-benzeri geni ISAba15 veya ISAba19 ile kesintiye uğrayabildiği için A.baumannii’nin tanısında blaOXA-51-benzeri genine özgül PCR yönteminin güvenilir olmadığı, yanlış negatif sonuçlar verebildiği bildirilmiştir[22],[23]. Ayrıca horizontal gen transferi ile A.baumannii olmayan türlerin blaOXA-51-benzeri geni kazanabileceği ve yanlış pozitif sonuçlara neden olabileceği gösterilmiştir[24].
Wang ve arkadaşları tarafından, blaOXA-51-benzeri geninin A.baumannii tanısında belirleyici olduğu bildirilen bir çalışmada[13], 2197 adet blaOXA-51-benzeri geni pozitif A.baumannii izolatından yalnızca birinde ISAba19 varlığı gösterilmiştir. Günümüze kadar gerçekleştirilen birçok çalışmada A.baumannii’nin tür düzeyinde tanımlanması için blaOXA-51-benzeri gen varlığının gösterilmesi, tek başına veya diğer gen bölgelerini hedef alan farklı bir moleküler yöntem ile birlikte kullanılmaktadır[18].
Bu çalışmada incelenen 180 Acb kompleks izolatının 177 (%98.3)’sinde blaOXA-51-benzeri geni saptanmış ve tümü ARDRA ve/veya MALDI-TOF yöntemi ile A.baumannii olarak tanımlanmıştır. blaOXA-51-benzeri geni saptanamayan üç izolat, ARDRA ve/veya MALDI-TOF yöntemi ile A.baumannii dışı olarak isimlendirilmiştir.
Son yıllarda; Acinetobacter cinsi içerisindeki türlerin tanımlanmasında blaOXA-51-benzeri gen bölgesinin yanı sıra 16S rRNA, 16S-23S rRNA ITS ve recA gibi çeşitli gen bölgelerini hedef alan PCR temelli yöntemler kullanılmaktadır. ARDRA; 16S rRNA geninin amplifikasyonu ve farklı restriksiyon enzimleri kullanılarak elde edilen fragmanların görüntülenmesi temeline dayanan ve Acinetobacter haemolyticus ile Acinetobacter johnsonii dışındaki tüm Acinetobacter türlerini tanımlayabilen bir yöntemdir[18].
Chang ve arkadaşları, Acb kompleks içerisindeki türlerin tanımlanmasında ARDRA’nın güvenilir bir yöntem olduğunu, ancak aynı türe ait farklı suşlar arasında birden fazla ARDRA profilinin görülebileceğini ve bu nedenle gram-negatif basillerin cins ya da tür düzeyinde tanımlanması için 16S rRNA’nın 527 bp gen sekansının yeterli olacağını bildirmişlerdir8. Bununla birlikte, Shehata ve arkadaşları[25] 81 klinik A.baumannii izolatını tiplendirdikleri çalışmalarında, ARDRA (kesim enzimleri: Alu I, Mbo I, Msp I) yönteminin ayırt edici gücünün düşük olduğunu belirtmişlerdir. ARDRA yöntemi, tekrarlanabilirlik ve sonuçların laboratuvarlar arası paylaşımı açısından çözülmemiş sorunları olmakla birlikte, Acinetobacter cinsi bakterilerin tür ayrımında doğru, hızlı ve kolay bir yöntem olarak birçok araştırmada kullanılmaktadır[26],[27].
Bu çalışmada, merkezlerde daha önce A.baumannii olarak tiplendirilmiş 180 izolattan 176’sı ARDRA ile A.baumannii, biri ise A.pittii olarak sonuçlandırılmıştır. Kalan üç örnekten blaOXA-51-benzeri geni pozitif bulunmuş olan bir örnek, MALDI-TOF yöntemi ile A.baumannii olarak tiplendirilmiştir (TR35). Sonuç olarak; blaOXA-51-benzeri gen varlığı ile ARDRA sonuçları uyumlu bulunmuş (179/180, %99.4) ve A.baumannii tür düzeyinde tanımlanması için referans yöntemler olarak blaOXA-51-benzeri genin PCR yöntemi ile gösterilmesi ve ARDRA yöntemleri birlikte kullanılmıştır.
MALDI-TOF, son yıllarda rutin tanı laboratuvarlarında giderek artan oranlarda kullanılan, bakterilerin cins, tür ve alt tür düzeyinde tanımlanmalarına olanak sağlayan bir tekniktir. Acb kompleks türlerinin tanımlanması için MALDI-TOF’un duyarlılık ve özgüllük değerlerinde farklılıklar olduğu görülmektedir. Bu farklılıkların nedeni genellikle çalışmalardaki yöntemsel farklılıklardan kaynaklanmaktadır. Örneğin bir çalışmada; geleneksel yöntemler ile duyarlılık %91, özgüllük %98 olarak rapor edilirken, bu oran bakteri kolonileri formik asit ve asetonitril ile modifiye ekstraksiyon uygulandığı zaman duyarlılık ve özgüllük değerlerinin %98’in üzerine yükseldiği rapor edilmiştir[19].
Espinal ve arkadaşları[14] tür düzeyinde tanımlanmış A.nosocomialis (n= 18), A.pittii (n=17), A.baumannii (n= 18) ve yedi farklı Acinetobacter türünü kullanarak MALDI-TOF (Bruker, ABD) veri setinin tanı performansını değerlendirmiş; referans suşlar için doğruluk oranını %85, A.baumannii için %100, A.pittii için ise %94 olarak bildirmişlerdir. Kan kültürü örneklerinden izole edilen Acinetobacter türlerinin değerlendirildiği bir başka çalışmada, VITEK® MS, VITEK® 2 ve MicroScan sistemleri için duyarlılık oranları, sırasıyla %90.3, %89.2 ve %86.9 olarak belirlenmiştir[28].
Bu çalışmada; MALDI-TOF’un Acinetobacter türlerinin tanımlanması için geçerlilik değerleri hesaplanmıştır. ARDRA ve Rt-PCR ile blaOXA-51-benzeri gen varlığının gösterilmesi teknikleri referans yöntemler olarak kabul edilmiştir. Toplam 180 izolat değerlendirilmiş ve MALDI-TOF’un duyarlılığı %99.3, özgüllüğü %75.0, doğruluk değeri %98.9 olarak bulunmuştur.
Sonuç olarak; rutin tanı laboratuvarlarında kullanılan konvansiyonel yöntemler ile karşılaştırıldığında, MALDI-TOF MS yönteminin Acinetobacter türlerini tam ve doğru bir şekilde tanımlayabilmesi için örnek başına 5 dakikadan daha kısa sürede izolatların %98’inden fazlasını daha düşük maliyetle ve daha yüksek doğruluk değeri ile tanımladığı izlenmiştir. MALDI-TOF yönteminin, veri tabanlarının geliştirilmesiyle, gelecekte rutin tanı laboratuvarlarında daha fazla türü tanımlayabilen, bakterilerde antibiyotik direnç ve virülans belirteçlerini test edebilen ideal bir sistem olacağını düşünmekteyiz.
ETİK KURUL ONAYI
Bu çalışma, Yıldırım Beyazıt Üniversitesi Klinik Araştırmalar Etik Kurulu onayı ile gerçekleştirildi (Tarih: 17.02.2016 ve Karar no: 33).
ÇIKAR ÇATIŞMASI
Yazarlar bu makale ile ilgili herhangi bir çıkar çatışması bildirmemişlerdir.
TEŞEKKÜR
Bu çalışma; TÜBİTAK 3001- Başlangıç Ar-Ge projeleri Destekleme Programı (proje no: 116S249) tarafından desteklenmiştir.
KAYNAKLAR
- List of Procaryotic names with Standing in Nomenclature. Genus Acinetobacter. https://lpsn.dsmz.de/genus/acinetobacter Erişim tarihi: 15.12.2019
- Gerner-Smidt P, Tjernberg I, Ursing J. Reliability of phenotypic tests for identification of Acinetobacter species. J Clin Microbiol 1991; 29(2): 277-82.
- Nemec A, Krizova L, Maixnerova M, Sedo O, Brisse S, Higgins PG. Acinetobacter seifertii sp. nov., a member of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex isolated from human clinical specimens. Int J Syst Evol Microbiol 2015; 65(Pt 3): 934-42.
- Cosgaya C, Marí-Almirall M, Van Assche A, Fernández-Orth D, Mosqueda N, Telli M, et al. Acinetobacter dijkshoorniae sp. nov., a member of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex mainly recovered from clinical samples in different countries. Int J Syst Evol Microbiol 2016; 66(10): 4105-11.
- Doi Y, Murray G, Peleg AY. Acinetobacter baumannii: evolution of antimicrobial resistance-treatment options. Semin Respir Crit Care Med 2015; 36(1): 85-98.
- Vaneechoutte M, Dijkshoorn L, Tjernberg I, Elaichouni A, de Vos P, Claeys G, et al. Identification of Acinetobacter genomic species by amplified ribosomal DNA restriction analysis. J Clin Microbiol 1995; 33(1): 11-5.
- Dijkshoorn L, Van Harsselaar B, Tjernberg I, Bouvet P J, Vaneechoutte M. Evaluation of amplified ribosomal DNA restriction analysis for identification of Acinetobacter genomic species. Syst Appl Microbiol 1998; 21(1): 33-9.
- Chang HC, Wei YF, Dijkshoorn L, Vaneechoutte M, Tang CT, Chang TC. Species-level identification of isolates of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex by sequence analysis of the 16S-23S rRNA gene spacer region. J Clin Microbiol 2005; 43(4): 1632-9.
- Yang Q, Rui Y. Two multiplex real-time PCR assays to detect and differentiate Acinetobacter baumannii and non-baumannii Acinetobacter spp. carrying blaNDM, blaOXA-23-like, blaOXA-40-like, blaOXA-51-like, and blaOXA-58like genes. PLoS ONE 2016; 11(7): e0158958.
- Lee MJ, Jang SJ, Li XM, Park G, Kook JK, Kim MJ, et al. Comparison of rpoB gene sequencing, 16S rRNA gene sequencing, gyrB multiplex PCR, and the VITEK2 system for identification of Acinetobacter clinical isolates. Diagn Microbiol Infect Dis 2014; 78(1): 29-34.
- Khosravi AD, Sadeghi P, Shahraki AH, Heidarieh P, Sheikhi N. Molecular methods for identification of Acinetobacter species by partial sequencing of the rpoB and 16S rRNA genes. J Clin Diagn Res 2015; 9(7): DC09-13.
- Turton J, Woodford N, Glover J, Yarde S, Kaufmann ME, Pitt TL. Identification of Acinetobacter baumannii by detection of the blaOXA-51-like carbapenemase gene intrinsic to this species. J Clin Microbiol 2006; 44(8): 2974-6.
- Wang J, Ruan Z, Feng Y, Fu Y, Jiang Y, Wang H, et al. Species distribution of clinical Acinetobacter isolates revealed by different identification techniques. PLoS ONE 2014; 9(8): e104882.
- Espinal P, Seifert H, Dijkshoorn L, Vila J, Roca I. Rapid and accurate identification of genomic species from the Acinetobacter baumannii (Ab) group by MALDI-TOF MS. Clin Microbiol Infect 2012; 18(11): 1097-103.
- Hou C, Yang S. Drug resistant gene of blaOXA-23, blaOXA-24, blaOXA-51 and blaOXA-58 in Acinetobacter baumannii. Int J Clin Exp Med 2015; 8(8): 13859-63.
- Woodford N, Ellington MJ, Coelho JM, Turton JF, Ward ME, Brown S, et al. Multiplex PCR for genes encoding prevalent OXA carbapenemases in Acinetobacter spp. Int J Antimicrob Agents 2006; 27(4): 351-3
- Nemec A, Krizova L, Maixnerova M, van der Reijden TJK, Deschaght P, Passet V, et al. Genotypic and phenotypic characterization of the Acinetobacter calcoaceticus-Acinetobacter baumannii complex with the proposal of Acinetobacter pittii sp. nov. (formerly Acinetobacter genomic species 3) and Acinetobacter nosocomialis sp. nov. (formerly Acinetobacter genomic species 13TU). Res Microbiol 2011; 162(4): 393-404.
- Vijayakumar S, Biswas I, Veeraraghavan B. Accurate identification of clinically important Acinetobacter spp.: an update. Future Sci OA 2019; 5(6): FSO395.
- Marí-Almirall M, Cosgaya C, Higgins PG, Van Assche A, Telli M, Huys G, et al. MALDI-TOF/MS identification of species from the Acinetobacter baumannii (Ab) group revisited: inclusion of the novel A.seifertii and A.dijkshoorniae species. Clin Microbiol Infect 2017; 3(3): 210.e1-210.e9.
- Brown S, Young HK, Amyes SGB. Characterisation of OXA-51, a novel class D carbapenemase found in genetically unrelated clinical strains of Acinetobacter baumannii from Argentina. Clin Microbiol Infect 2005; 1(1): 15-23.
- Evans BA, Amyes SGB. OXA -lactamases. Clin Microbiol Rev 2014; 27(2): 41-63.
- Zander E, Higgins PG, Fernández-González A, Seifert H. Detection of intrinsic blaOXA-51-like by multiplex PCR on its own is not reliable for the identification of Acinetobacter baumannii. Int J Med Microbiol 2013; 303(2): 88-9.
- Ahmadi A, Salimizand H. Delayed identification of Acinetobacter baumannii during an outbreak owing to disrupted blaOXA-51-like by ISAba19. Int J Antimicrob Agents 2017; 50(1): 119-22.
- Lee YT, Kuo SC, Chiang MC, Yang SP, Chen CP, Chen TL, et al. Emergence of carbapenem-resistant non-baumannii species of Acinetobacter harboring a blaOXA-51-like gene that is intrinsic to A.baumannii. Antimicrob Agents Chemother 2012; 56(2): 1124-7.
- Shehata AI, Al-Aidan AA, Al-Shahrani B, Al-Harbi NA, Alharbi SA. Typing of Acinetobacter baumannii strains isolated from hospital patients by amplified ribosomal DNA restriction analysis (ARDRA). Biosci Biotech Res Asia 2011; 8(2): 469-82.
- Ahmed SS, Alp E. Genotyping methods for monitoring the epidemic evolution of A.baumannii strains. J Infect Dev Ctries 2015; 9(4): 347-54.
- Gómez RF, Castillo A, Chávez-Vivas M. Characterization of multidrug-resistant Acinetobacter ssp. strains isolated from medical intensive care units in Cali - Colombia. Colomb Med (Cali) 2017; 48(4):1 83-90.
- Lee SY, Shin JH, Kim SH, Shin MG, Suh SP, Ryang DW. Evaluation of matrix-assisted laser desorption ionization-time of flight mass spectrometry-based VITEK MS system for the identification of Acinetobacter species from blood cultures: comparison with VITEK 2 and MicroScan systems. Ann Lab Med 2015; 35(1): 62-8.
İletişim (Correspondence):
Prof. Dr. Ayşegül Gözalan,
Alanya Alaaddin Keykubat Üniversitesi Tıp Fakültesi,
Tıbbi Mikrobiyoloji Anabilim Dalı,
Oba, Fidanlık Caddesi,07400 Alanya, Antalya, Türkiye.
Tel (Phone): +90 242 518 1144,
E-posta (E-mail): aysegul.gozalan@alanya.edu.tr,