İki Anti-HIV Doğrulama Testinin Karşılaştırılması: Rekombinant HIV 1/2 “Line İmmunoassay” ve Geenius HIV 1/2 Doğrulama Testi
Comparison of Two Anti-HIV Confirmatory Assays: Recombinant HIV 1/2 Line Immunoassay and Geenius HIV 1/2 Confirmatory Test
Ayşın ZEYTİNOĞLU1,Münevver KAYIN1,İmre ALTUĞLU1,Deniz GÖKENGİN2, Rüçhan SERTÖZ1
1 Ege Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, İzmir.
1 Ege University Faculty of Medicine, Department of Medical Microbiology, Izmir, Turkey
2 Ege Üniversitesi Tıp Fakültesi, Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı, İzmir.
2 Ege University Faculty of Medicine, Department of Infectious Diseases and Clinical Microbiology, Izmir, Turkey.
* Bu çalışma, Ege Üniversitesi Bilimsel Araştırma Birimi tarafından TGA-2018-20001 numaralı proje ile desteklenmiştir.
Makale Atıfı: Zeytinoğlu A, Kayın M, Altuğlu İ, Gökengin D, Sertöz R. İki anti-HIV doğrulama testinin karşılaştırılması: rekombinant HIV 1/2 “line immunoassay” ve geenius HIV 1/2 doğrulama testi. Mikrobiyol Bul 2020;54(4):613-618.
ÖZ
İnsan immün yetmezlik virüsü (HIV) enfeksiyonu tanısında temel amaç, hızlı ve doğru bir şekilde HIV enfeksiyonuna sahip kişilerin saptanmasıdır. Uluslararası ve ulusal rehberlerin klasik algoritmalarında tekrarlayan şekilde reaktif bulunan örneklerin doğrulanması/desteklenmesi gerektiği önerilmektedir. Uzun yıllardan beri kullanılan rekombinant “line immünoassay testi (LIA)”, maliyet ve emek etkin olması için biriktirilerek çalışılmaktadır. Bu çalışmada, rutin tanıda uzun süredir kullandığımız rekombinan HIV 1/2 LIA (INNO-LIA®, Fujirebio, Ghent, Belçika) ile daha hızlı sonuç verebilen, HIV-1 ve HIV-2 enfeksiyonu tanısının doğrulanması ve ayırt edilmesi için kullanılan immünokromatografik bir test olan Geenius™ HIV 1/2 doğrulama testi (Bio-Rad Laboratories, Marnes-la-Coquette, Fransa)nin karşılaştırılması amaçlanmıştır. Ege Üniversitesi Tıp Fakültesi Hastanesi Tıbbi Viroloji Laboratuvarına HIV serolojisinin değerlendirilmesi için gönderilen örneklerden anti-HIV 1/2 ve p24 antijen pozitif ve sınır değer saptanan 150 serum örneği ile HIV-1 pozitif olduğu bilinen üç dış kalite kontrol örneği olmak üzere toplam 153 örnek çalışmaya dahil edilmiştir. Enzim immün testlerle çalışılan örnekler, Geenius™ HIV 1/2 doğrulama (Bio-Rad Laboratories, Marnes-la-Coquette, Fransa) ve rekombinant HIV 1/2 LIA (INNO-LIA®, Fujirebio, Ghent, Belçika) testleri ile çalışıldı. HIV-1 viral yük sonuçları, plazma örneklerinde gerçek zamanlı HIV-1 testi ile Abbott m200sp sistem (Abbott Molecular, Wiesbaden, Almanya)’inde çalışılarak elde edilmiştir. Her iki doğrulama testinde sonuçlar 147 (%96.08) örnekte uyumlu bulunmuştur. Uyumsuz saptanan altı örneğin birinde LIA HIV-1 pozitif ve Geenius belirsiz, ikisinde LIA belirsiz ve Geenius HIV-1 pozitif, diğer üçünde de LIA belirsiz ve Geenius negatif saptanmıştır. HIV antikoru pozitif olan örneklerde LIA iki (2/97, %2.6) ve negatif olan üç (3/53, %5.66) örnekte belirsiz sonuç vermiştir. Geenius testi ise HIV antikoru pozitif ve negatif olan örnekleri doğru saptamıştır. Yeni kullanılmaya başlanan immünokromatografik test; uygulanma süresinin kısalığı, emek yoğun olmaması, HIV-1/2 ayrımını yapabilmesi, duyarlılık ve özgüllüğünün LIA ile karşılaştırıldığında yüksek olması ve her iki testin uyumlu olması ile tanı algoritmasında uygulanabilir olduğunu göstermektedir. Bu test de dahil olmak üzere tüm analitik antikor testlerinin akut HIV enfeksiyonu sırasında dördüncü kuşak enzim immünoassay testlerine göre enfeksiyonun daha geç döneminde pozitifleştiği akılda bulundurulmalıdır.
Anahtar kelimeler: Anti-HIV doğrulama testi; HIV line immunoassay; HIV immün kromatografi testi; hızlı HIV tanı testi
ABSTRACT
The main purpose in the diagnosis of human immunodeficiency virus (HIV) infection is to rapidly and accurately identify people with HIV infection. It is recommended that samples that are repeatedly reactive should be verified/supported according to the classical algorithms of international and national guidelines. The recombinant “line immunoassay test (LIA)”, which has been used for many years, is studied with the accumulated samples to be cost and labor-effective. In this study, the supplemental recombinant HIV 1/2 LIA (INNO-LIA®, Fujirebio, Ghent, Belgium) used to confirm and differentiate the diagnosis of HIV-1 and HIV-2 infections, and an immunochromatographic supplemental test (Geenius™ (Bio-Rad Laboratories, Marnes-la-Coquette, France) which can provide faster results were compared. One hundred fifty serum samples sent to Ege University Faculty of Medicine Hospital Medical Virology Laboratory with anti-HIV 1/2 and p24 antigen positive and indeterminant results and three HIV-1 positive external quality control samples were included in the study. Samples were tested both with the Geenius™ HIV 1/2 (Bio-Rad Laboratories, Marnes-la-Coquette, France) and recombinant HIV 1/2 LIA (INNO-LIA®, Fujirebio, Ghent, Belgium). HIV 1 viral load was evaluated by using Abbott real-time HIV-1 test in Abbott m200sp system (Abbott Molecular, Wiesbaden, Germany) in plasma samples. In both assays, the results were consistent in 147 samples (96.08%). Six samples that have discordant results were as follows: one sample was LIA HIV-1 positive and Geenius indeterminate, two samples were LIA indeterminant and Geenius HIV-1 positive, and in three samples, LIA was indeterminate and Geenius negative. In two EIA reactive samples (2/97, 2.06%) and three EIA negative samples (3/53, 5.66%) LIA results were indeterminant. Geenius test, on the other hand, correctly identified HIV positive and negative samples. The immunochromatographic test could be used in the diagnostic algorithm of HIV infection, due to its short application time, not being labor intensive, its ability to distinguish HIV-1/2, its high sensitivity/specificity compared to LIA, and the compliance with LIA. However, it should be noted that in acute HIV infection, all analytical antibody tests, become reactive later than the fourth generation enzyme immunoassays.
Keywords: Anti-HIV confirmatory assay; HIV line immunoassay; HIV immuno chromatography assay; rapid HIV diagnosis test
Geliş Tarihi (Received): 22.04.2020 - Kabul Ediliş Tarihi (Accepted):21.09.2020
GİRİŞ
Duyarlılık ve özgüllüğü yüksek testlerle insan immün yetmezlik virüsü [human immunodeficiency virus (HIV)]nün doğru laboratuvar tanısı, bu özellikleri taşıyan test algoritmalarına bağlıdır. Amerika Birleşik Devletleri Hastalık Kontrol ve Koruma Merkezleri [Centers for Disease Control and Prevention (CDC)] ve ulusal rehberlerimizin klasik algoritmalarında, tekrarlayan reaktif bulunan örneklerin doğrulanması/desteklenmesi önerilmektedir. Anabilim Dalımızda uzun yıllardan beri kullanılan rekombinant “line immünoassay (LIA)” testi, maliyet ve emek etkin olması için haftada bir gün çalışılmaktadır. Çalışma günü gelen örneklerin sonuçları en erken sekiz günde çalışılarak raporlanabildiğinden, sonuç verme süresi iki-sekiz gün arasında değişmektedir. Teknik bir sorun nedeni ile test tekrarı yapıldığında ise bu süre 15 güne çıkmaktadır.
Doğrulamada acil durumlarda kullanılabilecek hızlı HIV-1 RNA testlerinin kullanımı maliyet nedeni ile kısıtlıdır ve özellikle HIV-2 enfeksiyonu söz konusu ise bu testler yardımcı olamamaktadır. Değişik merkezlerde yapılan çalışmalarda, Geenius™ HIV 1/2 doğrulama testi (Bio-Rad Laboratories, Marnes-la-Coquette, Fransa)nin hızlı sonuç vermesi nedeni ile duyarlılık ve özgüllük sonuçlarına göre algoritmalardaki yeri araştırılmaktadır1.Bu çalışmada, rutin tanıda uzun süredir kullandığımız LIA ile daha hızlı sonuç verebilen, HIV-1 ve HIV-2 enfeksiyonu tanısının doğrulanması ve ayırt edilmesi için kullanılan immünokromatografik bir test olan Geenius HIV 1/2 doğrulama testinin karşılaştırılması amaçlanmıştır.
GEREÇ ve YÖNTEM
Bu çalışma, Ege Üniversitesi Klinik Araştırmalar Etik Kurul onayı (Tarih: 20.03.2013 ve Karar no: 18-3.1/70) ile Ege Üniversitesi Tıp Fakültesi Tıbbi Mikrobiyoloji Anabilim Dalı Tıbbi Viroloji Laboratuvarında gerçekleştirildi.
Laboratuvara gönderilen ve dördüncü kuşak kemilüminesan mikropartikül enzim immünolojik test [chemiluminescent microparticle immunoassay (CMIA)] Abbott ARCHITECT HIV Ag/Ab Combo Test [HIV p24 antijen + HIV-1 (M ve O grupları) ve HIV-2 antikorları], i2000SR cihazında (Abbott Laboratories, Abbott Park, IL, ABD) çalışılarak sınır değer ve pozitif bulunan; ardından aynı/farklı kitle iki kez enzim immün testte sınır değer ve pozitif elde edilen örnekler çalışmaya alındı. Örneklerin 101’i aynı sistemle (CMIA), 53’ü ise farklı bir sistemle [VIDAS® HIV Duo Ultra enzim bağlantılı floresan tekniği [enzyme-linked fluorescence assay (ELFA)], (HIV p24 antijen + HIV-1 (M ve O grupları) ve HIV-2 antikor sinyallerini ayrı olarak gösteren] (BioMérieux, Marcy l’Étoile, Fransa) çalışıldı. Bu tekrarlayan reaktif örnekler ve HIV-1 pozitif olduğu bilinen üç dış kalite kontrol örneği, Geenius™ HIV 1/2 doğrulama testi (Bio-Rad Laboratories, Marnes-la-Coquette, Fransa) ve rekombinant HIV 1/2 Line Immunoassay (INNO-LIA®, Fujirebio, Belçika) testi ile çalışılarak karşılaştırma yapıldı ve elde edilen sonuçlar değerlendirildi. Geenius HIV 1/2 doğrulama testi, üretici firma talimatları doğrultusunda çalışıldı2. Test, HIV-1 ve HIV-2 tanısı için gp160, gp41, p31, p24, gp140 ve gp36 antikorlarını araştırmakta ve yaklaşık 20-30 dakika içerisinde sonuç vermektedir. Rekombinant LIA ise HIV-1 ve HIV-2 tanısı için gp120, gp41, p31, p17, p24, gp105 ve gp36’ya karşı antikorları saptayabilen bir testtir ve 20 saat içerisinde sonuç vermektedir3. Test, HIV-1 viral yük sonuçları, plazma örneklerinde Abbott gerçek zamanlı HIV-1 testinin Abbott m2000sp (Abbott Molecular, Wiesbaden, Almanya) sisteminde kullanılarak elde edildi.
BULGULAR
Çalışmaya dahil edilen hastaların 105 (%70)’i erkek, 45 (%30)’i kadın olup yaşları 8 ay-75 yıl arasında bulunmuştur (ortalama= 37.4; ortanca= 35). Üç örnek ise dış kalite kontrol örneği olarak belirlenmiştir. Toplam 153 örneğin çalışılan doğrulama testleri karşılaştırıldığında, 51 örnekte her iki doğrulama testi “negatif”, 95 örnekte her iki doğrulama testi “anti-HIV-1 pozitif”, bir örnekte her iki doğrulama testi de “belirsiz (indeterminant)”, (altısında ise doğrulama testleri “uyumsuz” bulunmuştur. Her iki doğrulama testinde belirsiz çıkan sonuçlar tekrarlanmış ve aynı sonuçlar elde edilmiştir
Her iki doğrulama testinde sonuçlar 147 (%96.08) örnekte uyumlu bulunmuştur. Her iki doğrulama testinde negatif saptanan 51 örneğin üçünde bakılan HIV-1 RNA testi pozitif saptanmıştır. Bu üç olguda da ELFA testindeki pozitifliğin p24 antijeni nedeni ile olduğu ve HIV-1+2 antikorlarının negatif olduğu görülmüştür. Her iki doğrulama testi de belirsiz saptanan örnekte ELFA testinde p24 antijeni pozitif ve antikor negatif saptanmış olup her iki doğrulama testinde de altı gün sonra alınan örnek pozitifleşmiştir (HIV-1).
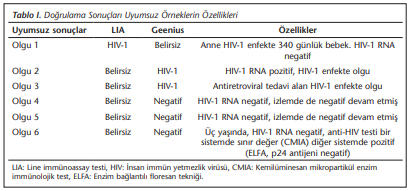
Uyumsuz saptanan altı örneğin birinde LIA HIV-1 pozitif ve Geenius belirsiz, ikisinde LIA belirsiz ve Geenius HIV-1 pozitif, diğer üçünde de LIA belirsiz ve Geenius negatif saptanmıştır. Uyumsuz sonuçların özellikleri (Tablo 1)’de görülmektedir.
Olgu 1’de azalmaya yüz tutmuş antikorları LIA HIV-1 olarak, Geenius ise belirsiz olarak saptamıştır. HIV-1 enfekte olan ikinci ve üçüncü olgular ile HIV enfekte olmayan dördüncü ve altıncı olgularda LIA testi belirsiz sonuç vermiştir. Tüm olguların değerlendirilmesinde HIV-1 RNA testi ve izlem yardımcı olmuştur (Tablo 1).
Klinik, HIV-RNA ve p24 antijen pozitifliği ile değerlendirilen olgular (n= 150), HIV antikoru pozitif (n= 97, üçü dış kalite kontrol örneği) ve HIV antikoru negatif (n= 53) olarak değerlendirilerek ayrılmıştır. Bu değerlendirmeye göre kullandığımız iki yöntem ile karşılaştırılmıştır.
Klinik, HIV-RNA ve p24 antijen ile enfeksiyon durumu izlenerek olgunun HIV enfekte olup olmadığı değerlendirilmiştir. Bu değerlendirmede, anneden geçen antikorların kaybolmaya başladığı dönemde alınan örnek nedeni ile antikoru pozitif olan, ancak HIV enfekte olmadığı için bir olgu ile diğeri akut enfeksiyonun erken döneminde p24 antijeni pozitif anti-HIV antikorunun yeni oluşmaya başladığı dönemde HIV antikor düzeyinin sınırlı olduğu iki olgu dışındakiler için doğrulama testlerinin değerlendirilmesi ayrıca yapılmıştır. Bu olguların birinde LIA’da HIV-1 antikor varlığı doğrulanırken, diğer olgu belirsiz sonuç vermiştir. Geenius her iki örnekte belirsiz sonuç vermiştir. Bu iki olguda, HIV-1 RNA ve izlem önerileceğinden, ileri incelemelerle olguların tanısı konulacaktır.
Testlerin her ikisinde de HIV antikoru pozitif olarak değerlendirilen olguların hiçbirinde negatiflik; HIV antikoru negatif olarak değerlendirilen olguların ise hiçbirinde pozitiflik saptanmamıştır. LIA, HIV antikoru pozitif olan örneklerin 2 (2/97, %2.06)’sinde, negatif olan örneklerin ise 3 (3/53, %5.66)’ünde belirsiz sonuç vermiştir. Geenius testi ise HIV antikoru pozitif ve negatif olan örnekleri doğru saptamıştır.
TARTIŞMA
HIV antikoru doğrulama/destekleme testi olan blot yöntemleri, kullanımda olan ELISA testlerine göre daha özgül fakat daha az duyarlıdır. Geenius HIV-1/2 hızlı testi, 2014 CDC HIV tanı rehberinde doğrulama testi olarak önerilmektedir[4]. Geenius testini “western blot (WB)” ile karşılaştıran bir çalışmada, testin HIV enfeksiyonunu destekleme ve dışlamada WB’ye göre üstünlükleri olduğu, testin özgüllüğünün %93, duyarlılığının ise WB’ye göre daha yüksek olduğu bildirilmiştir[5]. Bir diğer çalışmada, Geenius’un duyarlılığı %92, WB’nin %89 olarak saptanmıştır[6]. Moon ve arkadaşları, Geenius ile %100 duyarlılık elde etmiş ve testin, WB pozitif hiçbir örneği kaçırmadığını saptamışlardır[7]. Chiron RIBA, INNO LIA® ve multispot hızlı test ile karşılaştıran çalışmalarda, Geenius’un %99-100 özgüllük ve %96-100 duyarlılık ile bu testlerden üstün olduğu saptanmıştır[1],[8]-[11]. LIA ile karşılaştırıldığı bir diğer çalışmada, duyarlılık ve özgüllüğün daha düşük olduğu belirtilmiştir[12]. Çalışmamızda, HIV enfekte olan ve olmayan olgularda Geenius testinin özgüllük ve duyarlılığı %100 bulunmuştur. LIA testi, HIV enfekte olguların %2.06’sında, enfekte olmayan olguların ise %5.55’inde belirsiz sonuç vermiştir. Ancak, çalışmamızda belirsiz sonuç veren olguların kesin tanılarının, HIV-RNA ve izlemle konulduğu izlenmiştir. Bunun için her iki yöntemin de HIV tanısında yararlı olduğu görülmüştür..
Sonuç olarak, yeni kullanılmaya başlanan Geenius testi, uygulanma süresinin kısalığı, emek yoğun olmaması, HIV 1-2 ayrımını yapabilmesi, duyarlılık ve özgüllüğünün LIA ile karşılaştırıldığında yüksek olması ve her iki testin uyumunun %96.8 olması, testin tanı algoritmasında uygulanabilir olduğunu göstermektedir.
ETİK KURUL ONAYI
Bu çalışma, Ege Üniversitesi Klinik Araştırmalar Etik Kurul onayı ile gerçekleştirildi (Tarih: 20.03.2013 ve Karar no: 18-3.1/70).
ÇIKAR ÇATIŞMASI
Yazarlar bu makale ile ilgili herhangi bir çıkar çatışması bildirmemişlerdir.
KAYNAKLAR
- Malloch L, Kadivar K, Putz J, Levett PN, Tang J, Hatchette TF et al. Comparative evaluation of the Bio-Rad Geenius HIV-1/2 Confirmatory Assay and the Bio-Rad Multispot HIV-1/2 Rapid Test as an alternative differentiation assay for CLSI M53 algorithm-I. J Clin Virol 2013: 58 (S1); e85-e91.
- Bio-Rad2013. Geenius HIV 1/2 confirmatory assay. No. 883601-2013/01. Bio-Rad Laboratories, Marnes-la-Coquette, France.
- Fujirebio Europe. 2015. INNO-LIA HIV I/II score. No. 28672 V4-2015-10-06. Fujirebio Europe N.V., Ghent, Belgium.
- Centers for Disease Control and Prevention (CDC). Laboratory testing for the diagnosis of HIV infection: updated recommendations. June 2014; Available from: https://stacks.cdc.gov/view/cdc/23447 Erişim tarihi:10.03.2020
- Serhir B, Desjardins C, Doualla-Bell F, Simard M, Tremblay C, Longtin Ja. Evaluation of the Bio-Rad Geenius HIV 1/2 Assay as Part of a Confirmatory HIV Testing Strategy for Quebec, Canada: Comparison with Western Blot and Inno-Lia Assays. J Clin Microbiol 2019; 57 (6): e01398-18.
- Montesinos I, Eykmans J, Delforge ML. Evaluation of the Bio-Rad Geenius HIV-1/2 test as a confirmatory assay. J Clin Virol 2014; 60:399-401.
- Moon HW, Huh HJ, Oh GY, Lee SG, Lee A, Yun YM, et al. Evaluation of the Bio-Rad Geenius HIV 1/2 confirmation assay as an alternative to Western blot in the Korean population: a multi-center study. PLoS One 2015; 10: e0139169.
- Tuaillon E, Sanosyan A, Pisoni A, Liscouet J, Makinson A, Perre PV. Staging of recent HIV-1 infection using Geenius rapid confirmatory assay compared to INNO-LIA, New Lav, and Blot 2.2 assays. J Clin Virol 2017; 95: 47-51.
- Friedrichs I, Buus C, Berger A, Keppler OT, Rabenau HF. Evaluation of two HIV antibody confirmatory assays: Geenius HIV1/2 confirmatory assay and the recomLine HIV-1 & HIV-2 IgG line immunoassay. J Virol Methods 2015; 224: 91-4.
- Mor O, Mileguir F, Michaeli M, Levy I, Mendelson E. Evaluation of the Bio-Rad Geenius HIV 1/2 assay as an alternative to the INNO-LIA HIV 1/2 assay for confirmation of HIV infection. J Clin Microbiol 2014; 52(7): 2677-9.
- Fordan S, Bennett B, Lee M, Crowe S. Comparative performance of the Geenius HIV-1/HIV-2 supplemental test in Florida’s public health testing population. J Clin Virol 2017; 91: 79-83.
- Tinguely C, Schild-Spycher T, Bahador Z, Gowland P, Stolz M, Niederhauser C. Comparison of a conventional HIV 1/2 line immunoassay with a rapid confirmatory HIV 1/2 assay. J Virol Methods 2014; 206: 1-4.
İletişim (Correspondence):
Prof. Dr. Ayşın Zeytinoğlu,
Ege Üniversitesi Tıp Fakültesi,
Tıbbi Mikrobiyoloji Anabilim Dalı,
35100 Bornova, İzmir,
Tel (Phone):+90 232 390 3303 ,
E-posta (E-mail): selmagk@gmail.com,