Genişlemiş Spektrumlu Beta-Laktamaz Üreten
Enterik Bakterilerde Fosfomisin Duyarlılığının Disk Difüzyon,
Otomatize Sistem ve Agar Dilüsyon Kiti ile Araştırılması
Investigation of Fosfomycin Susceptibility
in Extended Spectrum Beta-Lactamase Producing Enteric Bacteria
by Disk Diffusion, Automated System and Agar Dilütion Kit
Gizem SOYDAN , Yusuf GÖRGÜLÜ , Candan ÖZTÜRK
Mersin Üniversitesi Tıp Fakültesi, Tıbbi Mikrobiyoloji Anabilim Dalı, Mersin.
Mersin University Faculty of Medicine, Department of Medical Microbiology, Mersin, Turkey.
Makale Atıfı:Soydan G, Görgülü Y, Öztürk C. Genişlemiş spektrumlu beta-laktamaz üreten enterik bakterilerde fosfomisin duyarlılığının disk difüzyon, otomatize sistem ve agar dilüsyon kiti ile araştırılması. Mikrobiyol Bul 2021;55(4):617-625.
ÖZ
Son yıllarda klasik antibiyotiklere direnç geliştiren bakterilerin artması nedeniyle fosfomisin, yeniden önem kazanan antibiyotikler arasına girmiştir. Fosfomisin, pek çok bakteri üzerine olan bakterisidal etkisini sitoplazmik bir enzim olan MurA’ya bağlanarak ve peptidoglikan sentezinde yer alan enolpürivil transferaz enzimini inhibe ederek gösterir. Genişlemiş spektrumlu beta-laktamaz (GSBL) üreten bakteriler, nozokomiyal enfeksiyonlarda sık izole edilen patojenlerdir ve tedavilerinde sıklıkla dirençle karşılaşılmaktadır. Fosfomisinin etki spektrumu içerisinde bulunan, bu bakterilerle gelişen enfeksiyonların tedavisinde, fosfomisin alternatif bir tedavi seçeneği olarak görülmektedir. Yeniden kullanıma girmesiyle, fosfomisin için güvenilir ve tekrarlanabilir duyarlılık test yöntemleri oluşturmak önemlidir. Bu çalışmada, GSBL üreten enterik bakterilerin fosfomisin duyarlılığının disk difüzyon, otomatize MicroScan sistemi ve agar dilüsyon kiti ile belirlenmesi ve bu yöntemlerin fosfomisin duyarlılığını belirlemede kullanılabilirliklerinin değerlendirilmesi amaçlamıştır. Çalışmaya Mayıs 2019-Kasım 2019 tarihleri arasında Mersin Üniversitesi Tıp Fakültesi Hastanesi Mikrobiyoloji Laboratuvarına gönderilen örneklerde üreyen, GSBL pozitif 120 enterik bakteri (89 Escherichia coli ve 31 Klebsiella pneumoniae) izolatı dahil edilmiştir. Çalışmaya dahil edilen izolatların fosfomisin duyarlılıkları; disk difüzyon, otomatize MicroScan sistemi (Beckman Coulter, Brea, CA, ABD) ve agar dilüsyon kiti ile test edilmiştir. Çalışmada disk difüzyon yöntemiyle 120 izolatın 37 (% 30.8)’si; MicroScan otomatize sistemiyle 6 (%5)’sı fosfomisine dirençli bulunmuştur. Fosfomisin duyarlılığını belirlemede agar dilüsyon kiti ile 120 izolatın 11 (%9.1)’i minimal inhibitör konsantrasyon (MİK) değerinin > 32 µg/ml olması nedeniyle dirençli olarak tespit edilmiştir. Agar dilüsyon ile fosfomisin direnci, K.pneumoniae izolatlarında E.coli izolatlarına göre anlamlı derecede yüksek bulunmuştur (p= 0.006). Yüz yirmi izolatın yedisinde ertapenem direnci saptanmıştır. Ertapeneme dirençli bulunan yedi izolatın tamamı, agar dilüsyon yöntemiyle fosfomisine duyarlı bulunmuştur. Kolistine dirençli saptanan üç izolatın tamamı da, agar dilüsyon ile fosfomisine duyarlı bulunmuştur. Çalışmada, disk difüzyon ve MicroScan yöntemlerinin E.coli izolatlarında, agar dilüsyon kiti ile kategorik uyumu yüksek ve hata oranları düşük hesaplanmıştır. K.pneumoniae izolatları için, kategorik uyumu disk difüzyon testi için %22.5 ve MicroScan için %74.1 olarak hesaplanırken, büyük ve küçük hata oranları oldukça yüksek olarak bulunmuştur. Sonuç olarak, fosfomisinin, GSBL üreten enterik bakteriler üzerine yüksek etkinliğiyle, özellikle karbapenem ve kolistin dirençli bakterilerin neden olduğu enfeksiyonların tedavisinde alternatif bir ilaç seçeneği olabileceği düşünülmüştür. E.coli için fosfomisin direncinin tespitinde agar dilüsyon yöntemi ile MicroScan ve disk difüzyon yöntemi arasında büyük oranda uyum olduğu, agar dilüsyon yöntemine göre maliyet ve iş gücü açısından kullanım kolaylığı sağlayan disk difüzyon yönteminin güvenilir bir yöntem olarak kullanılabileceği tespit edilmiştir. Ancak K.pneumoniae izolatlarında fosfomisin duyarlılık testi için standart yöntem olan agar dilüsyon yönteminin kullanılması gerektiği yeniden ortaya konmuştur. Buna rağmen agar dilüsyon yapılamayan laboratuvarlarda otomatize sistem kullanılırsa, hata oranlarının çok yüksek olmasından dolayı sonuçların dikkatli yorumlanması gerektiği sonucuna varılmıştır.
Anahtar kelimeler: Fosfomisin; Enterobacterales; duyarlılık; agar dilüsyon.
ABSTRACT
Due to the increase of bacteria that develop resistance to classical antibiotics in recent years, fosfomycin has become one of the antibiotics gaining importance again. Fosfomycin exerts its bactericidal effect on many bacteria by binding to a cytoplasmic enzyme, MurA, and inhibiting the enzyme enopurivil transferase, which is involved in peptidoglycan synthesis. Bacteria producing ESBL are common pathogens in nosocomial infections and resistance is frequently encountered in their treatment. Fosfomycin is considered as an alternative drug in these infections. With its reintroduction, it is important to establish reliable and reproducible susceptibility testing methods for fosfomycin. In this study, it was aimed to evaluate the utility of disk diffusion, agar dilution kit and automated MicroScan methods (Beckman Coulter, Brea, CA, ABD) for fosfomycin susceptibility of ESBL-producing enteric bacteria. The study included 120 ESBL positive isolates of enteric bacteria (89 Escherichia coli, 31 Klebsiella pneumoniae) cultivated from the samples sent to the Microbiology Laboratory of the Mersin University Medical Faculty of Medicine Hospital between May 2019 and November 2019. Fosfomycin susceptibilities of the isolates included in the study were tested by disk diffusion, automated MicroScan and the commercial agar dilution kit. In the study, 37 (30.8%) of 120 isolates were determined as resistant to fosfomycin by disk diffusion method and six (5%) of the isolates were found to be resistant to fosfomycin with the MicroScan automatized system. With the agar dilution kit, 11 (9.1%) of 120 isolates were found to be resistant as the minimum inhibitory concentration (MIC) values were > 32 µg/ml. Fosfomycin resistance was significantly higher in K.pneumoniae isolates than E.coli isolates by agar dilution method (p= 0.006). Ertapenem resistance was detected in seven of 120 isolates. All seven isolates that were resistant to ertapenem were susceptible to fosfomycin by agar dilution method. All three isolates, which were found resistant to colistin, were susceptible to fosfomycin by agar dilution method. In the study, the categorical agreement of the disk diffusion and MicroScan methods in E.coli isolates with the agar dilution was high and the error rates were low. For K.pneumoniae, categorical concordance was calculated as 22.5% for disk diffusion test and 74.1% for MicroScan, while major and minor error rates were found to be quite high. As a result; fosfomycin is thought to be an alternative drug option in the treatment of infections caused by especially carbapenem and colistin resistant bacteria, with its high activity on ESBL-producing enteric bacteria. It has been determined that there is a great agreement between the agar dilution, which is the reference method for the determination of fosfomycin resistance for E.coli, and the MicroScan and disk diffusion methods, and that the disk diffusion method which provides ease of use in terms of cost and labor compared to the agar dilution method, can be used as a reliable method. However, it has been demonstrated that the agar dilution method should be used in K.pneumoniae isolates. Nevertheless; It was concluded that if the automatized system is used in laboratories where agar dilution cannot be performed, the results should be interpreted carefully, since the error rates are very high.
Keywords: Fosfomycin; Enterobacterales; susceptibility; agar dilution..
Geliş Tarihi (Received): 21.12.2020 - Kabul Ediliş Tarihi (Accepted):22.06.2021
GİRİŞ
Enterik bakteriler nozokomiyal enfeksiyonlarda en sık izole edilen patojenlerdir. Bu bakterilerle gelişen enfeksiyonların tedavilerinde de antibiyotik direnci nedeniyle güçlük yaşanmaktadır[1]. Tedavi zorluğunun en önemli nedenlerinden biri, bu bakterilerin ürettiği genişlemiş spektrumlu beta-laktamaz (GSBL) enzimidir[2]. GSBL üreten bakteriler penisilinlere, geniş spektrumlu sefalosporinlere ve aztreonama karşı direnç oluşumuna neden olmaktadır[3]. Karbapenemler, GSBL üreten enterik bakterilerle gelişen invaziv enfeksiyonlarda ilk tercih olarak görülmektedir. Ancak sık karbapenem kullanımının oluşturduğu karbapenem direnci riski nedeniyle kullanımı sınırlı tutulmaya çalışılmaktadır[4]. Bu nedenle GSBL üreten bakterilerin neden olduğu enfeksiyonların tedavilerinde farklı antibiyotik seçenekleri aranmaktadır.
Fosfomisin; bakterilerde sitoplazmik bir enzim olan MurA (UDP-GlcNAc enolpürivil transferaz)’ya bağlanarak peptidoglikan sentezini bozar ve pek çok bakteri üzerine bakterisidal etki gösterir[5],[6],[7]. Çok ilaca dirençli bakterilerle oluşan enfeksiyonlara karşı, yeni ilaç arayışları sonucu yeniden kullanıma giren fosfomisin, GSBL üreten enterik bakterilere karşı iyi bir antimikrobiyal seçenek olarak görülmektedir[8]. Kullanıma girmesiyle birlikte, fosfomisin için etkin ve güvenilir antibiyotik duyarlılık testlerine gereksinim vardır. Fosfomisin duyarlılığını belirlemek için Klinik ve Laboratuvar Standartları Enstitüsü [Clinical and Laboratory Standards Institute (CLSI)] ve Avrupa Antimikrobiyal Duyarlılık Testi Komitesi [the European Committee on Antimicrobial Susceptibility Testing (EUCAST)] tarafından çeşitli öneriler yayımlanmıştır. CLSI, yalnızca idrardan izole edilen E.coli ve Enterococcus faecalis izolatları için fosfomisin duyarlılığı belirlemede disk difüzyon yönteminin kullanılabileceğini belirtmekte ve referans yöntem olarak agar dilüsyon yönteminin kullanılmasını önermektedir. EUCAST ise idrardan izole edilen E.coli izolatları için disk difüzyon yöntemini; diğer Enterobacterales türleri ve idrar dışı E.coli izolatlarında ise MİK belirlenmesi gerektiğini ve referans yöntem olarak da agar dilüsyon yönteminin kullanılmasını önermiştir. EUCAST, 2020 güncellenmesinden önce sıvı mikrodilüsyon ya da agar dilüsyon yöntemleri fosfomisin duyarlılığını belirlemede altın standart olarak kabul edilmişken son güncellenmeden sonra sıvı mikrodilüsyon, fosfomisin duyarlılığını belirlemek için önerilmemiş, referans yöntem olarak agar dilüsyon yöntemi tavsiye edilmiştir[9],[10],[11]. Bunların dışında fosfomisin duyarlığını belirlemede otomatize sistemler ve antibiyotik gradiyent difüzyon testleri kullanılabilmektedir ancak bu yöntemler henüz standart yöntemler içerisinde yer almamaktadır.
Bu çalışmada Mersin Üniversitesi Tıp Fakültesi Hastanesi Mikrobiyoloji Laboratuvarına gönderilen örneklerde üreyen, GSBL üreten enterik bakterilerde fosfomisin duyarlılığının; disk difüzyon, otomatize MicroScan (Beckman Coulter, Brea, CA, ABD) sistemi ve ticari agar dilüsyon kiti ile belirlenmesi ve yöntemlerin uyumlarının değerlendirilmesi amaçlanmıştır.
GEREÇ ve YÖNTEM
Bu çalışma, Mersin Üniversitesi Klinik Araştırmalar Etik Kurulu onayı ile gerçekleştirildi. (Tarih: 03/04/2019 ve Karar No: 2019/156).
Çalışmaya Mayıs 2019-Kasım 2019 tarihleri arasında Mersin Üniversitesi Tıp Fakültesi Hastanesi Mikrobiyoloji Laboratuvarına gönderilen örneklerden izole edilen GSBL enzimi ürettiği fenotipik yöntemlerle tespit edilen 120 enterik bakteri izolatı dahil edildi. Laboratuvarımıza gelen klinik örnekler, %5 koyun kanlı agar (Oxoid, İngiltere) ve EMB (Oxoid, İngiltere) besiyerlerine ekilerek 24-48 saat, 35-37˚C’de aerobik koşullarda inkübe edildi. Üreyen kolonilerin tanımlanması ve GSBL tespiti konvansiyonel yöntemlerle ve ek olarak otomatize MicroScan sistemiyle belirlendi. Çalışmaya dahil edilen izolatlar, %20 gliserollü buyyonda, derin dondurucuda saklandı.
İzolatların fosfomisin direnç durumunu belirlemek için saklamaya alınmış izolatlar, %5’lik koyun kanlı agara pasajlandı. İzolatların fosfomisin duyarlılık testleri, Kirby-Bauer disk difüzyon yöntemi, MicroScan Walkaway Plus 96 (Beckman Coulter, Brea, CA, ABD) otomatize sistemi ve fosfomisin agar dilüsyon kiti ile çalışıldı.
Disk difüzyonla fosfomisin duyarlılık testi, Kirby-Bauer disk difüzyon yöntemiyle Mueller-Hinton agar kullanılarak EUCAST önerilerine göre yapıldı. Üreyen kolonilerinden 0.5 McFarland standart bakteri süspansiyonu hazırlandı ve Mueller-Hinton agara inoküle edildikten sonra fosfomisin 200 μg (Bioanalyze, Türkiye) antibiyotik diski petri plağına yerleştirildi. Petri plakları 37˚C’de 18-24 saat inkübasyona bırakıldıktan sonra inhibisyon zon çapları EUCAST önerilerine göre değerlendirildi. Fosfomisin zon çapı≥ 24 mm olanlar duyarlı, < 24 mm olanlar dirençli olarak kabul edildi.
İzolatların otomatize MicroScan sistemiyle fosfomisin duyarlılığını belirlemek için NM44 antibiyogram kartları kullanılarak üretici firma önerileri doğrultusunda fosfomisin MİK değerleri belirlendi.
Fosfomisin duyarlılığını belirlemede referans yöntem olan agar dilüsyon için, EUCAST standartlarına uygun hazırlandığı belirtilen ve içerisinde fosfomisinin 0.25-256 µg/ml seri konsantrasyonunu içeren Mueller-Hinton agar bazlı ticari fosfomisin agar dilüsyon kiti (Liofilmchem, İtalya) kulanıldı. Kit kullanılırken üretici firma önerileri doğrultusunda, saf koloni halindeki izolattan 0.5 McFarland bulanıklık ayarında koloni süspansiyonu hazırlanarak 900 µl serum fizyolojik içeren ayrı bir tüpe 100 µl aktarıldı. Böylece 1/10 oranında seyreltilmiş bakteri süspansiyonu hazırlandı. Bu bakteri süspansiyonundan her bir kuyucuğa 2 µl olacak şekilde mikropipet yardımıyla agar yüzeyine bırakılarak ekim yapıldı. Agar yüzeyindeki inokülum, besiyeri tarafından absorbe olana kadar havada kurutuldu. 37˚C’de 24 saat inkübasyon sonrasında kuyucuklar siyah zemin üzerinde değerlendirildi. Üremenin olmadığı ilk kuyucuğun karşılık geldiği konsantrasyon MİK değeri olarak belirlendi. MİK≤ 32 µg/ml duyarlı olan izolatlar duyarlı; > 32 µg/ml olan izolatlar dirençli kabul edildi. Agar dilüsyonla MİK belirlemeye bir örnek Şekil 1’de gösterildi.
İstatistiksel Analiz
Verilerin istatistiksel analizi SPSS 22 paket programı ile yapıldı. Kategorik yapıdaki değişkenlerin analizleri için ki-kare testi kullanıldı. İstatistiksel olarak anlamlılık kriteri (p değeri) 0.05 olarak belirlendi.
BULGULAR
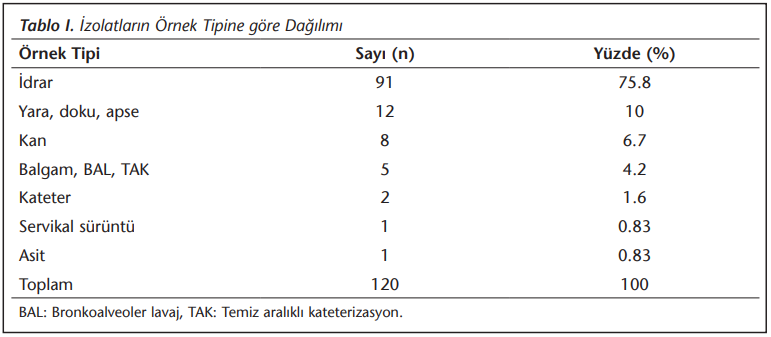
Çalışmaya dahil edilen GSBL pozitif 120 izolatın 89 (%74.2)’u E.coli, 31 (%25.8)’i K.pneumoniae olarak tanımlanmıştır. İzolatların %52.5’i polikliniklerden; %29.1’i çeşitli servislerden ve %18.4’ü yoğun bakım ünitelerinden gelen örneklerden izole edilmiştir. Çalışmaya dahil edilen 120 izolatın örnek tipine göre dağılımı Tablo 1’de gösterilmiştir. EUCAST tarafından E.coli idrar izolatları için önerilen sınır değerlere göre 120 izolatın fosfomisin için disk difüzyon testi değerlendirilmiştir. E.coli idrar dışı örnekler ve Klebsiella spp. türleri için sınır değer EUCAST’ta yayımlanmadığı için tüm izolatlar E.coli idrar örneklerinin kriterlerine göre değerlendirilmiş ve agar dilüsyon kiti ile uyumu araştırılmıştır. EUCAST önerilerine göre < 24 mm zon çaplı izolatlar dirençli; ≥ 24 mm zon çaplı izolatlar duyarlı olarak kabul edilmiştir. Buna göre; 120 izolattan 37 (% 30.8)’si disk difüzyon yöntemiyle dirençli bulunmuştur.
MicroScan otomatize sistemiyle 120 izolattan 6 (%5)’sı dirençli olarak bulunmuştur. Dirençli izolatların hepsinin MİK değeri > 64 µg/ml olarak raporlanmıştır. Dirençli bulunan altı izolatın üçü E.coli, üçü K.pneumoniae olarak tanımlanmıştır.
İzolatların otomatize sistemle aynı zamanda sefalosporinlere, kinolon grubu antibiyotiklere, ertapeneme ve kolistine direnç durumu da değerlendirilmiştir. Toplam 120 izolatın 72’si siprofloksasin ve levofloksasinin ikisine birden dirençli bulunurken; 38’i ikisine birden duyarlı olarak bulunmuştur. K.pneumoniae ile E.coli izolatları arasında kinolon duyarlılığı açısından anlamlı bir fark bulunmamıştır (p= 0.528). Referans yönteme göre değerlendirilen fosfomisin duyarlılığına bakıldığında 72 izolatın izolatların yalnızca altısı fosfomisine dirençli bulunurken, 66 izolat fosfomisine duyarlı bulunmuştur.
Karbapenem grubundan ertapeneme direnç; 120 izolatın yedi tanesinde saptanmıştır. Ertapeneme dirençli saptanan yedi izolatın tamamı (%100) fosfomisin agar dilüsyon kiti ile duyarlı bulunmuştur.
İzolatların kolistin duyarlılığı değerlendirildiğinde; 120 izolatın üçü kolistine dirençli saptanmış ve izolatlar K.pneumoniae olarak tanımlanmıştır. Bu üç izolatın, fosfomisin agar dilüsyon MİK değeri 16 µg/ml olarak tespit edilmiş ve fosfomisine duyarlı bulunmuştur.
Agar dilüsyon kiti ile 120 izolatın 11 (%9.1)’inde MİK değeri > 32 µg/ml olarak bulunmuş ve fosfomisine dirençli oldukları tespit edilmiştir. Bu izolatların yedisinin K.pneumoniae ve dördünün E.coli olduğu saptanmıştır. K.pneumoniae izolatlarında E.coli izolatlarına oranla, fosfomisin agar dilüsyon kiti ile test edilen direnç oranı istatistik açıdan anlamlı olarak yüksek bulunmuştur (p= 0.006). Dirençli saptanan izolatlarda poliklinik, servis yoğun bakımdan gelen örnekler arasında ve idrar ve idrar dışı örnekler arasında anlamlı fark saptanmamıştır (p= 0.411, p= 0.132).
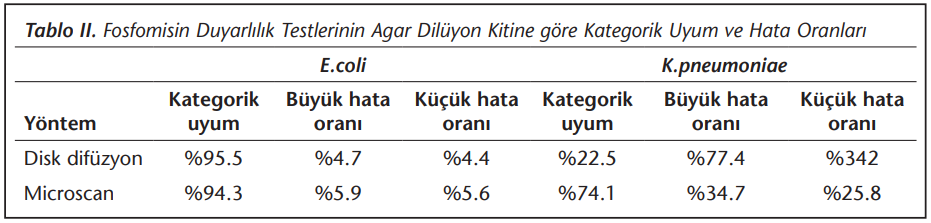
Çalışmada kullanılan fosfomisin duyarlılık yöntemlerinden disk difüzyon ve MicroScan yöntemlerinin; agar dilüsyon kitine göre kategorik uyum, büyük ve küçük hata oranları Tablo 2’de gösterilmiştir.
TARTIŞMA
GSBL enzimi üreten bakterilerle gelişen enfeksiyonların tedavilerinde güçlük yaşanmaktadır[2]. Bu nedenle, bu tür enfeksiyonlar için yeni ilaç arayışları devam etmektedir[4]. Bu çalışmada, hastanemiz Mikrobiyoloji Laboratuvarına gönderilen ve GSBL üreten örneklerde fosfomisin duyarlılığı; disk difüzyon, otomatize MicroScan ve agar dilüsyon kiti ile çalışılmıştır. Çalışmaya dahil edilen GSBL pozitif 120 izolattan, 89 (%74.2)’u E.coli, 31(%25.8)’i K.pneumoniae olarak tanımlanmıştır.
Ülkemizden bildirilen, disk difüzyon ve sıvı mikrodilüsyon yöntemiyle fosfomisin duyarlılığının araştırıldığı bir çalışmada 302 E.coli izolatının tamamı fosfomisine duyarlı olarak bildirilmiştir[12]. Ülkemizde ve farklı ülkelerde gerçekleştirilen, E.coli izolatlarında disk difüzyon yöntemiyle fosfomisin direncinin araştırıldığı çeşitli çalışmalarda direnç oranı, %5’in altında bildirilmiştir[12],[13],[14],[15],[16]. Çalışmamızda disk difüzyon ile E.coli izolatlarının %6.8’i fosfomisine dirençli bulunmuştur. Bu oran literatüre yakın olmasına rağmen yıllar içinde fosfomisine direncin arttığını düşündürmüştür.
Çalışmamızda K.pneumoniae izolatlarının tamamı disk difüzyon yöntemi ile fosfomisine dirençli bulunmuştur. Linsenmeyer ve arkadaşlarının çalışmalarında[17], Klebsiella türlerinde disk difüzyon ile fosfomisine %51 oranında direnç bildirilmiştir. Çalışmamızdaki Klebsiella izolatlarında disk difüzyonla bulunan yüksek direnç oranı, diğer çalışmalarda kullanılan CLSI kriterlerinde fosfomisin zon çapı ≥ 16 mm olan izolatların duyarlı kabul edilmesiyle açıklanabilir. Çalışmamızda Klebsiella izolatlarında, EUCAST E.coli suşlarının zon çapı değerleri kullanıldığı için, diğer çalışmalara oranla daha yüksek direnç saptandığı düşünülmüştür.
Bielen ve arkadaşlarının çalışmasında[18], fosfomisinin gram-negatif izolatlara karşı, karbapeneme kıyasla daha yüksek aktiviteye sahip olduğu vurgulanmıştır. Çalışmamızda da, 120 izolatın yedisi ertapeneme dirençli bulunmuş ve bu izolatların tamamı, agar dilüsyon ile fosfomisine duyarlı bulunmuştur. Buna göre, GSBL üreten bakterilerle gelişen enfeksiyonların tedavilerinde fosfomisinin karbapenemlere alternatif olabileceği düşünülmüştür.
Hirsch ve arkadaşlarının çalışmasında[16], agar dilüsyon ile E.coli izolatlarının tamamı fosfomisine duyarlı bulunurken, Klebsiella spp. izolatları %95.5 oranında duyarlı olarak bildirilmiştir. Çalışmamızda, E.coli izolatlarında agar dilüsyon ile fosfomisin duyarlılığı %95.6, K.pneumoniae izolatlarında %77.5 olarak bulunmuştur. Çalışmamızda, Klebsiella izolatlarında E.coli izolatlarına göre fosfomisin direnci anlamlı olarak yüksek bulunmuştur. Linsenmeyer ve arkadaşları[17] da benzer şekilde Klebsiella izolatlarında E.coli izolatlarına göre anlamlı düzeyde yüksek direnç bildirmişlerdir.
Çalışmamızda fosfomisin duyarlılığını belirlemede, E.coli için disk difüzyon yönteminin agar dilüsyon ile kategorik uyumu %95.5 iken, MicroScan otomatize sistemi için bu oran %94.3 bulunmuştur. E.coli izolatlarında, her iki yöntemde de kategorik uyumun %90’nın üzerinde çıkması, bu yöntemlerin fosfomisin duyarlılığı belirlemede kullanılabileceğini göstermektedir. E.coli için disk difüzyonun agar dilüsyon ile kategorik uyumunun daha yüksek olması ve hata oranlarının daha düşük olması nedeniyle agar dilüsyonun gerçekleştirilemediği laboratuvarlarda, disk difüzyon yönteminin kullanılması önerilebilir. K.pneumoniae izolatlarında; kategorik uyum, disk difüzyon testi için %22.5 ve MicroScan için %74.1 olarak hesaplanmış ve iki yöntem için de hata oranları oldukça yüksek olarak bulunmuştur. E.coli izolatlarına oranla görülen düşük uyumun sebebi K.pneumoniae için EUCAST tarafından belirlenen bir zon çapı olmadığı için, E.coli sınır değerleri kullanılması olarak yorumlanmıştır.
Çalışmamızın kısıtlılığı; konvansiyonel agar dilüsyon yerine ticari agar dilüsyon kiti kullanılmasıydı. Konvansiyonel agar dilüsyonun zahmetli ve zaman alıcı bir yöntem olması nedeniyle, ticari fosfomisin agar dilüsyon kiti tercih edilmiştir. Bununla birlikte çalışmamız; bu kitin kullanıldığı, ülkemizden bildirilen ilk çalışma niteliğindedir. Kullanılan bu kitin, EUCAST standartlarına uygun olarak hazırlandığı bildirilmiştir ve yurt dışından bildirilen diğer çalışmalarda da, standart agar dilüsyon yöntemiyle uyumlu olduğu gösterilmiştir[19],[20]. Bu nedenle çalışmamızda referans yöntem olarak agar dilüsyon kiti ile karşılaştırma yapılmıştır.
Sonuç olarak fosfomisinin, GSBL üreten enterik bakteriler üzerine yüksek etkinliğiyle, dirençli bakterilerin neden olduğu enfeksiyonların tedavisinde alternatif bir ilaç olabileceği düşünülmüştür. E.coli için fosfomisin direncinin tespitinde referans yöntem olan agar dilüsyon ile MicroScan ve disk difüzyon yöntemleri arasında büyük oranda uyum olduğu, agar dilüsyona göre maliyet ve iş gücü açısından avantaj sağlayan disk difüzyon yönteminin güvenilir bir yöntem olarak kullanılabileceği düşünülmüştür. K.pneumoniae izolatlarında ise, fosfomisin duyarlılığı belirlemede agar dilüsyon yönteminin kullanılması gerektiği yeniden ortaya konmuştur. Bununla birlikte, agar dilüsyon yöntemi uygulanamayan mikrobiyoloji tanı laboratuvarlarında otomatize sistem kullanılması halinde, hata oranının çok yüksek olması nedeniyle sonuçların dikkatli yorumlanması gerektiği sonucuna varılmıştır.
ETİK KURUL ONAYI
Bu çalışma, Mersin Üniversitesi Klinik Araştırmalar Etik Kurulu onayı ile gerçekleştirildi. (Tarih: 03/04/2019 ve Karar No: 2019/156).
ÇIKAR ÇATIŞMASI
Yazarlar bu makale ile ilgili herhangi bir çıkar çatışması bildirmemişlerdir.
KAYNAKLAR
- Bozkurt H, Kurtoğlu MG, Aygül K, Bayram Y, Berktaş M. Nozokomiyal kaynaklı Klebsiella pneumoniae ve Escherichia coli izolatlarında genişletilmiş spektrumlu beta laktamaz üretimi. Turk Med J 2007; 1: 150-3.
- Bradford PA. Extended-spectrum -lactamases in the 21st century: characterization, epidemiology, and detection of this important resistance threat. Clin Microbiol Rev 2001; 14(4): 933-51.
- Paterson DL, Bonomo RA. Extended-spectrum beta-lactamases: a clinical update. Clin Microbiol Rev 2005; 18(4): 657-86.
- Pana ZD, Zaoutis T. Treatment of extended spektrum beta laktamase producing what we have learned until now? F1000Res 2018; 1:1347.
- Aghamali M, Sedighi M, Bialvei AZ, et al. Fosfomycin: mechanisms and the increasing prevalence of resistance. J Med Microbiol 2019; 68(1): 11-25.
- Ramos JR, Lleti MS. Fosfomycin in infections caused by multidrug-resistant gram-negative pathogens. Rev Esp Quimioter 2019; 32(1):45-54.
- Baylan O. Fosfomisin: dünü, bugünü ve geleceği. Mikrobiyol Bul 2010; 44(2): 311-21.
- Falagas ME, Kanellopoulou MD, Karageorgopoulos DE. Antimicrobial susceptibility of multidrug-resistant gram-negative bacteria to fosfomycin. Eur J Clin Microbiol Infect Dis 2008; 27(6): 439-43.
- Doern CD. Fosfomycin susceptibility testing. Clin Microbiol Newsletter 2020; 42: 4.
- The European Committee on Antimicrobial Susceptibility Testing. Breakpoint tables for interpretation of MICs and zone diameters. Version 10.0, 2020. Available from: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Breakpoint_tables/v_10.0_Breakpoint_Tables.pdf
- Díez-Aguilar M, Cantón R. New microbiological sspects of fosfomycin. Rev Esp Quimioter 2019; 32(Suppl 1): 8-18.
- Süzük-Yıldız S, Kaştepe B, Avcıküçük H, Sanal L, Erdem G, Çöplü N. Escherichia coli idrar izolatlarında sıvı mikrodilüsyon yöntemi ile fosfomisin duyarlılığının belirlenmesi ve üriner sistem enfeksiyonlarında sık kullanılan diğer antibiyotiklerle karşılaştırılması. Turk Hij Den Biyol Derg 2018; 75(1): 29-36.
- Mengeloğlu FZ, Demircan F, Oduncu MK. İdrar kültürlerinden soyutlanan Escherichia coli izolatlarının fosfomisine karşı in-vitro duyarlılıklarının değerlendirilmesi. ANKEM Derg 2011; 25(2): 99-102.
- Demir T, Buyukgoclu T. Fosfomycin: in vitro efficacy against multidrug-resistant isolates beyond urinary isolates. J Glob Antimicrob Resist 2017; 8: 164-8.
- Fournier D, Chirouze C, Leroy J, Cholley P, Talon D, Plésiat P, et al. Alternatives to carbapenems in ESBL-producing Escherichia coli infections. Med Mal Infect 2013; 43(2): 62-6.
- Hirsch EB, Raux BR, Zucchi PC, Kim Y, McCoy C, Kirby JE, et al. Activity of fosfomycin and comparison of several susceptibility testing methods against contemporary urine ısolates. Int J Antimicrob Agents 2015; 46(6): 642-7.
- Linsenmeyer K, Styrims J, Weir S, Berg G, Brecher S, Gupta K. Activity of fosfomycin against extended-spectrum--lactamase-producing uropathogens in patients in the community and hospitalized patients. Antimicrob Agents Chemother 2016; 60(2): 1134-6.
- Bielen L, Likić R, Erdeljić V, Firis N, Marijana Grgić-Medić Ö, Godan A, et al. Activity of fosfomycin against nosocomial multiresistant bacterial pathogens from Croatia: a multicentric study. Croat Med J 2018; 59(2): 56-64.
- Parisio EM, Camarlinghi G, Coppi M, Niccolai C, Antonelli A, Nardone M, et al. Evaluation of the commercial AD fosfomycin test for susceptibility testing of multidrug-resistant Enterobacterales and Pseudomonas aeruginosa. Clin Microbiol Infect 2021; 788: e5-e9.
- Campanilea F, Woottonb M, Daviesb L, Aprile A, Mirabile A, Pomponio S, et al. Gold standard Susceptibility testing of fosfomycin in Staphylococcus aureus and Enterobacterales using a new agar dilution panel. J Glob Antimicrob Resist 2020; 23 :334-7.
İletişim (Correspondence):
Dr. Gizem Soydan,
Mersin Üniversitesi Tıp Fakültesi,
Tıbbi Mikrobiyoloji Anabilim Dalı,
Çiftlikköy Kampüsü 33343 Yenişehir/Mersin, Türkiye.
Tel (Phone):+90 (324) 241 0000/22393,
E-posta (E-mail):gizem.soydan33@gmail.com